This is an old revision of the document!
Table of Contents
Etiologie duševních poruch
Etiologie z řeckého αἰτία (příčina) a λογία (věda) – Věda o příčínách
Patogeneze z řeckého πάθος (zážitek/utrpení/nemoc), γένεσις (geneze, stvoření) – Vývoj nemoci
Etiopatogeneze – příčina vzniku a vývoje nemoci
U většiny duševních poruch není etiologie zatím objasněná a je předmětem současného výzkumu. Je ale jasné, že jen velmi málo duševních poruch má jednu jasnou a známou příčinu (monofaktoriální etiologie). Např. organická halucinóza podmíněna nádorem v mozku nebo Huntingtonova choroba podmíněna mutací genu pro huntingtin. U většiny psychických poruch mluvíme o multifaktoriální etiologii. Porucha vzniká z mnoha spolu interagujících příčin.
Etiologická klasifikace duševních poruch (v hledisku dnešních poznatků příliš zjednodušující) nám může poskytnout základní představu čím můžou být psychické potíže jedince způsobeny:
- Organické duševní poruchy - duševní poruchy způsobené tělesným onemocněním, nebo poškozením mozkové tkáně na základě hrubšího impaktu (infekce, nádory, úrazy, poruchy hormonální a metabolické, úbytek mozkové tkáně)
- Poruchy vyvolané užíváním psychoaktivních látek - nerovnováha způsobená toxickým působením psychoaktivních látek
- Psychózy: takový stav ve kterém je narušený kontakt s realitou, často se vyskytují bludy a halucinace (vědomí nebývá porušeno), příčinou je specifická dysfunkce mozku, ne však taková, jako u organických poruch..
- Afektivní poruchy: poruchy nálady, příčinou je specifická dysfunkce mozku jiná než u organických poruch, kontakt s realitou je zachován.
- Neurózy: porucha vzniká na základě vnitřních konfliktů a komplexů, projevuje se v zátěžových a vztahových situacích zejména úzkostí. Kontakt s realitou je zachován.
- Reakce: Porucha je vázaná na nepříznivé události v životě a na nezvládnutí stresové situace.
- Poruchy osobnosti: Osobnost se vyvinula atypicky a způsobuje okolí a jedinci setrvalé vztahové a mezilidské obtíže.
Faktory vzniku psychických poruch dle úrovně, na které je sledujeme:
Biologické - poškození jednotlivých anatomických struktur mozku (nádory, ischemie, krvácení, úrazy), postižení funkčních systémů (sítí) mozku (infekce, intoxikace, hypoxie, dehydratace, metabolické postižení…), buněčné a molekulární postižení (genetické odchylky, odchylky v neuroplasticitě, odchylky v neurotransmisi)
Psychologické - patologicky vyvinutá osobnost, nízká úroveň saturace citových a materiálních potřeb v dětství, patologický styl navazování mezilidských vazeb (attatchment), traumatizace, naučené dysfunkční vzorce chování a kognitivní schémata, nedostatečná psychická odolnost (rezilience) vůči nepříznivým vlivům okolí, nízká úroveň emoční regulace, nízká frustrační tolerance, atd.
Sociální - finanční strádání, nezaměstnanost, osamělost, nekvalitní poškozující vztahy, mezilidské konflikty, společenské vyčleňování (příslušnost k minoritním skupinám), stigmatizace, tranzitorní krize a změny společenských rolí.
Ekologické - životní styl, nedostatečná nebo přílišná smyslová a kognitivní stimulace, stresová zátěž, střídání ročních období
Spirituální - absence uplatnění, životních cílů, zájmů, jednání inkongruentní s vlastními hodnotami, absence životního smyslu a existenciální prázdno.
Jednotlivé úrovně faktorů způsobujících duševní poruchy se vzájemně ovlivňují a potencují co může vést k tzv. cirkulární kauzalitě, kdy vznikají začarované (bludné) kruhy (“circus vitiosus”) na sebe vzájemně navázaných procesů, které se potencují v zhoršování stavu. To ale zároveň znamená, že je možné k psychickým poruchám léčebně přistupovat na různých úrovních, které pak můžou působit i na ostatní úrovně.
Faktory vzniku psychických poruch dle období jejich působení:
- Predisponující
- Vrozené (působící před narozením)
- genetické faktory
- faktory prenatálního vývoje (infekce, užívání návykových látek, stres matky, teratogeny)
- porodní komplikace (perinatální poškození plodu- hypoxie, poranění…)
- Vývojové (působící během vývoje mozku od dětství do rané dospělosti)
- infekce, hypoxie, úrazy a jiné nemoci mozku v dětství a dospívání
- příliš nízká nebo příliš vysoká úroveň saturace citových a materiálních potřeb
- traumatizace (týrání, zanedbávání péče, zneužívání, vztahové trauma, šikana)
- patologické vzorce chování a patologická kognitivní schémata v primární rodině
- časné odloučení od matky
- rozvod rodičů, smrt rodiče
- psychická porucha nebo abusus psychoaktivních látek u rodiče
- užívání psychoaktivních látek a léků
- Setrvalé (působící dál během života na základě predisponujících faktorů a životních okolností)
- odchylky v neuroplasticitě a v neurotransmisi mozku
- odchylky v osobnostní struktuře (nedostatečná psychická odolnost (rezilience) vůči nepříznivým vlivům okolí, nízká úroveň emoční regulace, nízká frustrační tolerance, patologický způsob vztahování k okolí, specifické vzorce přemýšlení a chování)
- faktory životního stylu (tendence k zneužívání návykových látek, nedostatečný pohyb, přílišný pohyb, nevyvážená strava, nedostatek spánku, absence režimu, chaotičnost)
- faktory životních okolností (nezaměstnanost, osamělost, finanční strádání, tíživá rodinná situace aj.)
- Kritické (faktory vyvolávající (spouštějící) psychickou poruchu na více nebo méně predisponovaném terénu)
- somatické onemocnění (infekce, nádor, iktus, endokrinní, metabolická, úraz)
- intoxikace psychoaktivní látkou (jednorázová/ opakovaná)
- střídání ročních období
- tranzitorní krize- změny životních rolí (přechod do dospělosti, z VŠ do zaměstnání, do důchodu, narození dítěte)
- vztahové krize (rozchod, rozvod, úmrtí blízkého)
- ztráta zaměstnání
- zadlužení
- vyhoření (soustavné přetěžování)
- psychotrauma ale i mimořádně pozitivní životní události
Faktory vzniku psychických poruch dle jejich původu:
- endogenní (vnitřní): např. mozkové nádory, ischemie, epilepsie, roztroušená skleróza, endokrinní porucha, celková hypoxie, dehydratace
- exogenní (vnější): intoxikace, úrazy hlavy, infekce aj.
Protektivní faktory (faktory preventivní a pozitivně ovlivňující vývoj psychických poruch):
- podpůrné bezpečné blízké vztahy
- životní styl (režim, kvalitní spánek, abstinence od psychoaktivních látek, vyvážená strava, pravidelný pohyb)
- ekonomická stabilita (bydlení, práce, absence dluhů)
- pocit smysluplnosti života (víra, jednání na základě hodnot, smysluplné zájmy, zastávání smysluplných životních rolí, pocit užitečnosti druhým)
- adherence k psychoterapii a farmakoterapii
Biologické faktory
V této kapitole je popis anatomických, buněčních a molekulárních struktur, chemických systémů mozku a jejich vztah k duševním onemocněním.
Biologická psychiatrie popisuje
- patologické procesy v mozku doprovázející duševní poruchy
- mechanizmus působení psychofarmak a psychoaktivních substancí
Základy funkční neuroanatomie
Centrální nervová soustava (mozek a mícha) je řídící centrum organismu. Její základním cílem je udržet homeostázu organizmu. Zpracovává informace z vnějšího a vnitřního prostředí, které se k ní dostávají a na základě nich vytváří a reguluje odpověď. Funguje rovněž jako prediktor stavů na základě asociace signálů (např. u podmíněných reflexů).
Mozek se skládá z vzájemně propojených neuronových sítí a funkčních drah mezi nimi vzniklých. Šedá hmota obsahuje těla neuronů (viz níže) a dendrity a bílá hmota obsahuje zejména axony s myelinovými pochvami. Shluky těl neuronů s určitou specifickou funkcí a propojením k ostatním částem mozku nazýváme jádra (nucleus - nuclei/ ncl.).
Jednotlivé mozkové struktury a jejich propojení jsou mimo jiné biologickým základem psychických funkcí (vědomí, paměti, myšlení, emočních reakcí, kognitivního zpracovávání dějů, vnímání…). Narušení jejich struktury, nebo funkce má korelát v projevech psychických funkcí. Specifický druh jejich narušení hraje roli u duševních poruch.
(zdroj obrázků a info mimo uvedené zdrojeWikiskriptaHopkins Medicine)
Anatomické rozčlenění CNS nesleduje jeho funkční členění, některé funkční systémy a celky mají součásti z několika oddílů mozku:
- Mícha
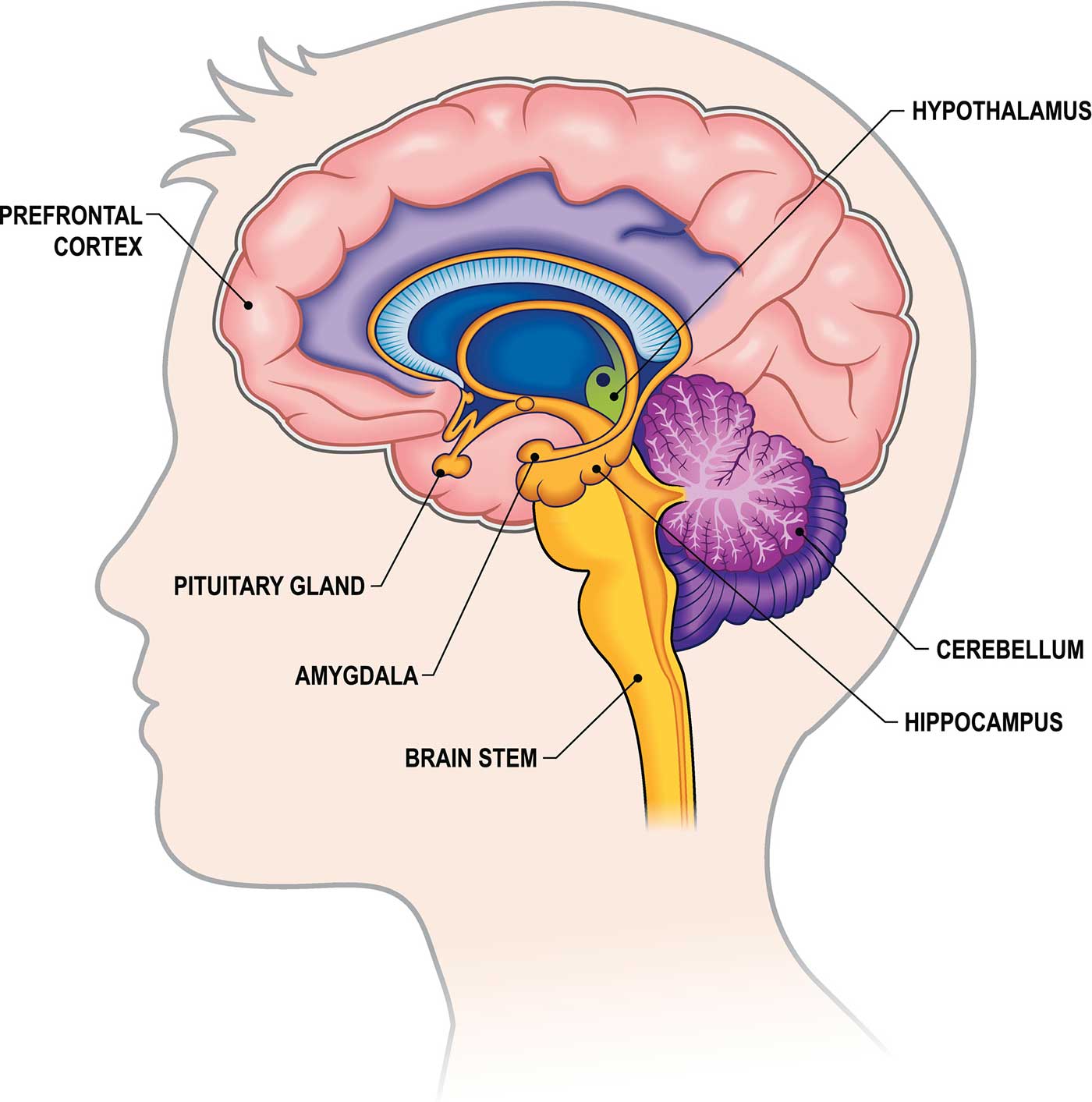
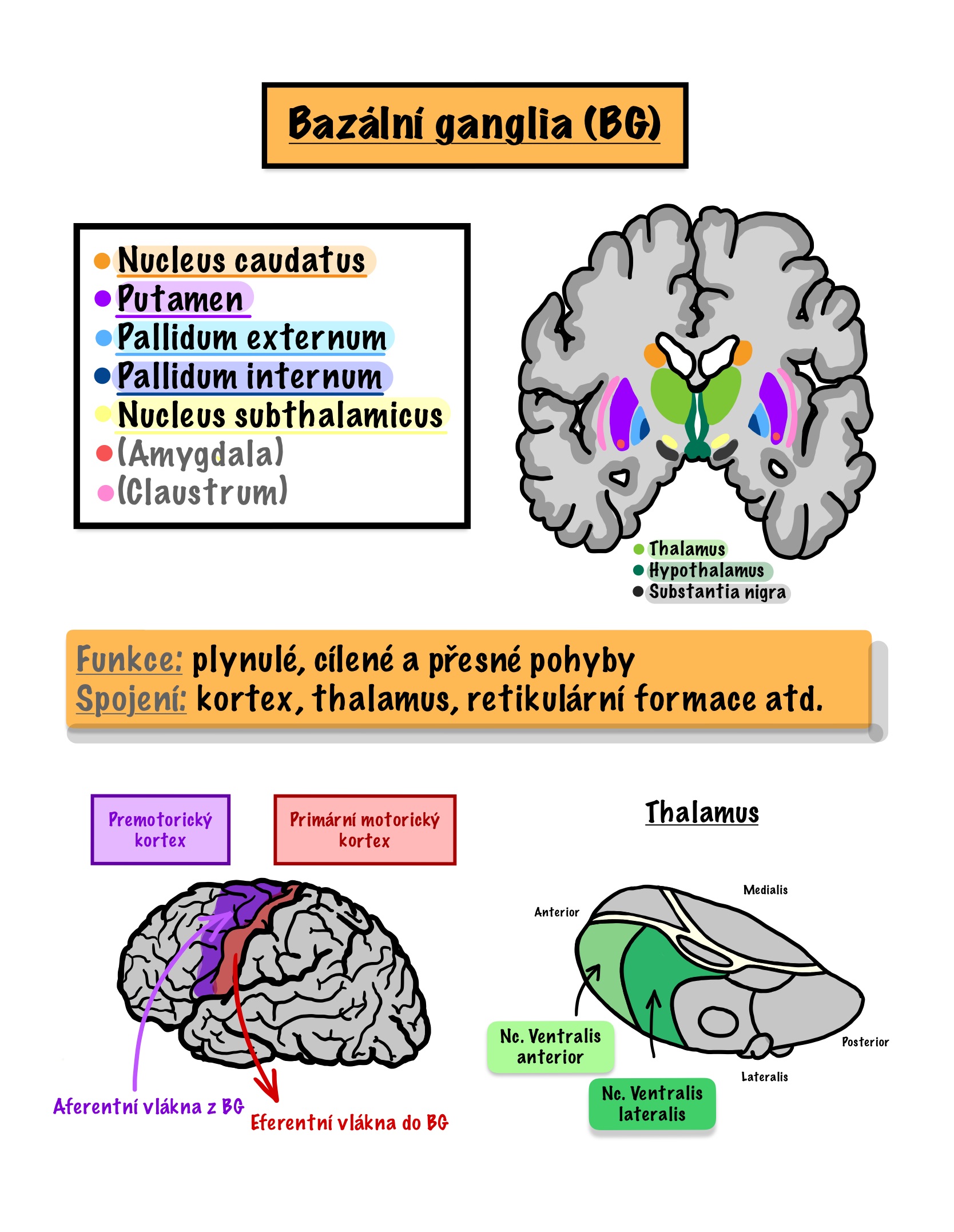
- Mozkový kmen (prodloužená mícha, varolův most- pons varoli, střední mozek- mesencephalon) na obrázku žlutě
- Mozeček - cerebellum
- Mezimozek – diencephalon (epithalamus, thalamus, metathalamus, subthalamus a hypothalamus) na obrázku tmavě modrá
- Koncový mozek – telencephalon
Prodloužená mícha - je nutná k přežití, reguluje srdeční tep, dýchání, proudění krve, hladiny kyslíku a oxidu uhličitého, reflexy jako kašel, kýchání, zvracení, polykání.
Pons (varolův most) – jsou zde jádra 12 hlavových nervů regulující svaly obličeje, cit v obličeji, sluch, držení rovnováhy etc.
Střední mozek (Mesencephalon) – složitá struktura, jsou zde jádra a nervové dráhy sloužící k regulaci různých funkcí, sluch, pohyb, odpovědi na vnější podněty, jsou zde důležitá jádra ventrální tegmentální area (VTA) a substantia nigra (SN) bohaté na dopaminergní (dopamin produkující) neurony, kterých dráhy mají vliv na vznik závislosti a schizofrenie, dále degenerativní porušení SN vede k M. Parkinson. Mesencephalon obsahuje periakveduktální šeď, starou strukturu, která vysílá signály do amygdaly o bolesti. (stilmulací lze vyvolat panické ataky, bývá zbytnělá při panické poruše)
Mozeček (Cerebellum) - má dvě hemisféry. Hlavní funkcí je udržování stability chůze a stoje, regulace a vyrovnávání volných pohybů (inhibice). Studuje se jeho role v regulaci emocí a sociálního chování.
PODKOROVÉ STRUKTURY - MEZIMOZEK - diencephalon
Hypofýza - hlavní hormonální žláza řídící funkci ostatních hormonálních žláz v těle (štítnou žlázu -TSH thyreostimulační hormon, nadledvinky - ACTH adrenokortikotropní hormon, ovaria (vaječníky) FSH- folikulostimulační hormon, varlata - LH -luteinizační hormon), vylučuje prolaktin, růstový hormon, oxytocin, ADH -antidiuretický hormon. Její funkce je řízená z hypothalamu.
Hypothalamus - nachází se nad hypofýzou a řídí její funkci (vylučuje stimulující hormony - CRH -kortikoliberin, gonadoliberin GnRH, thyreoliberin TRH, a inhibiční hormony např. dopamin, který inhibuje vylučování prolaktinu z hypofýzy (tuberoinfundibulární dráha), nebo somatostatin inhibující výdej růstového hormonu), je to rovněž nejvyšší inegrační a řídící centrum autonomního nervového systému, reguluje tělesnou teplotu, synchronizuje spánkové rytmy, kontroluje hlad a žízeň, hraje roli v některých aspektech emocí (libost a nelibost při naplnění/nenaplnění určitého motivačního úsilí) a paměti.
Thalamus - nazývá se též “brána vědomí”, obsahuje jádra, kde se integrují a převádí signály z nižších oddílů mozku (mícha, kmen, mozeček, bazální ganglia) do mozkové kůry. Děje v mozku odehrávající se subthalamicky (které neprojdou thalamem do kůry) si neuvědomujeme. Některá jeho jádra jsou součástí limbického systému.
Amygdala - mandlový útvar nacházející se v hloubce temporálního laloku. Má roli v řízení emocí, paměti, je spojená se stresem, strachem a agresí. Aktivuje se při stresu a spouští reakci “Fight” or “flight”. Je to takový mozkový alarm. Reaguje na signály i potenciálního ohrožení. Míra její reakce je regulovaná z prefrontální kůry kognitivně - myšlením - když kognitivně vyhodnotíme že se o ohrožující podnět nejedná, tak se její reakce ztiší. Naopak, když kognitivně vyhdonotíme, že se jedná o ohrožující podnět, může se její signál zesílit. Reaguje na podněty rychleji než prefrontální kůra. Pokud je regulace kortexu oslabená, nebo je amygdalová reaktivita zesílená, vede to k zvýšené citlivosti a stresové reakci na neutrální podněty.
Normálně, když nás něco poleká (např. neočekávané hlasité bouchutí dveří), na pár sekund se nám rozbuší srdce, zalije nás vlna napětí, ztuhnou nám svaly, toto spouští amygdala. Když ten vjem doputuje do prefrontálního kortexu a my si uvědomujeme, že to jenom bouchli dveře a všechno je v pořádku, a zklidníme se, ten signál, že je všechno v pořádku vysílá do amygdaly prefrontální kortex.
Amygdalická dysregulace je základem například PTSD (posttraumatické stresové poruchy), kdy na zdánlivě neohrožující podněty ale paměťově spojené s traumatizující událostí spouští stresovou reakci.
Základem kognitivně behaviorální terapie úzkostných poruch je zesilování prefrontální regulace amygdalické stresové odpovědi změnou v myšlení.
Hipokampus – orgán ve tvaru mořského koníka na spodu temporálního laloku je součástí hippokampální formace, řídí paměť, učení, vnímání a navigaci v prostoru, dostává informace z kortexu a z vnitřního prostředí (má v sobě kortikoidní receptory), hraje roli v regulaci stresové odpovědi. Často bývá jeho objem zmenšený u dlouhodobého stresu, deprese.
Šišinka- nachází se hluboko v mozku a je připojená kmínkem na vrcholu třetí mozkové komory. Reaguje na světlo a tmu a vylučuje melatonin- hormon aktivující spánek, regulující cirkadiánní rytmy a cyklus spánek/bdění.
- Limbický systém - velmi složitý, vzájemně propojený komplex různých struktur nacházejících se na mediální ploše mozkové hemisféry po obou stranách mezimozku shora obepnutý corpus callosum. Patří sem mimo jiné amygdala, septum verum, hypotalamus, některá jádra thalamu atd. Nejdůležitější funkce je kontrola strachu, úzkosti, sociálního a emočního chování, libých emocí, podílí se na krátkodobé paměti, a díky napojení na hypothalamus řízení srdeční činnosti, dechové frekvence, a sekrece endokrinních žláz.
KONCOVÝ MOZEK- telencephalon
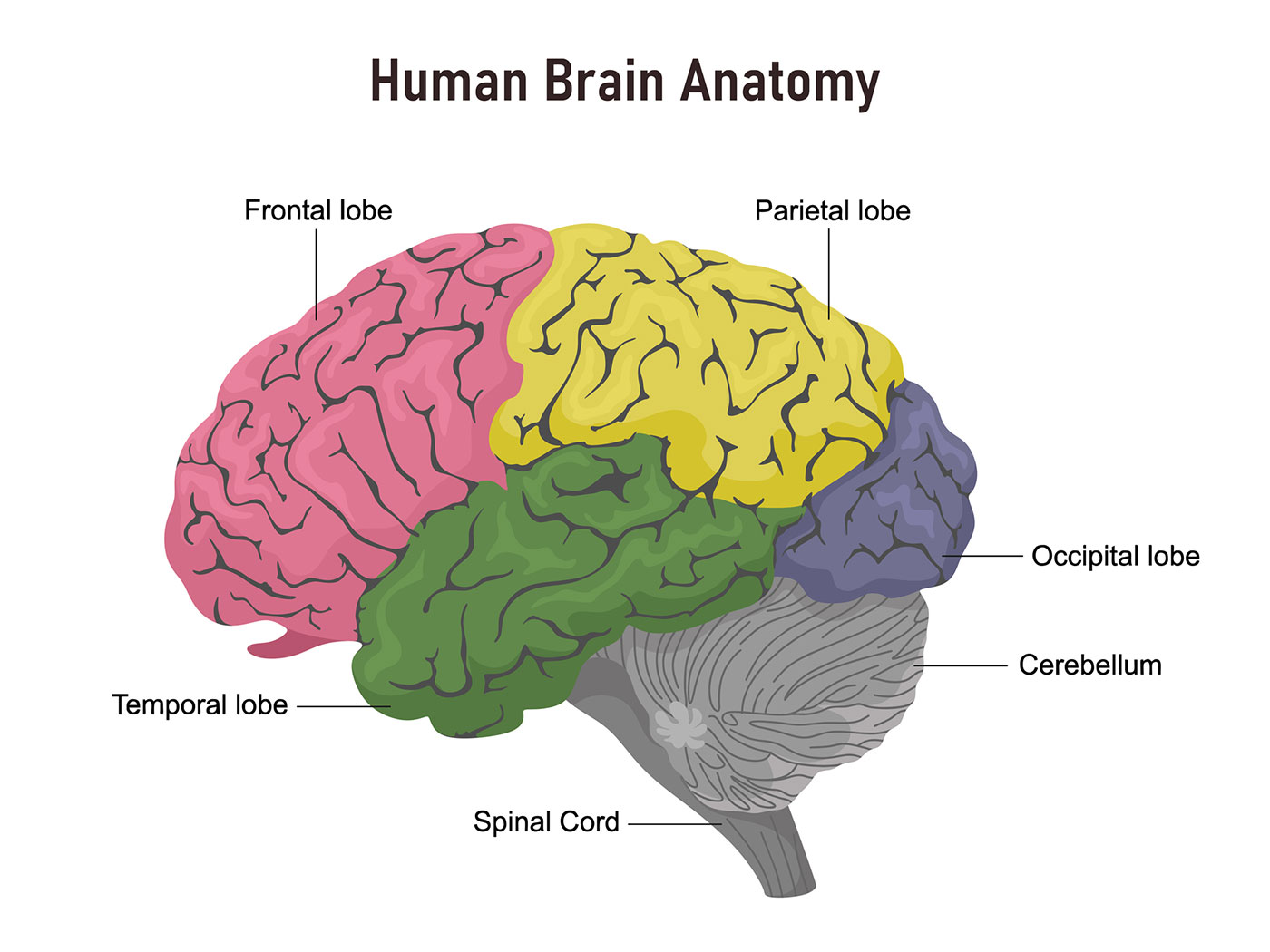
Skládá se ze dvou hemisfér pravá a levá ze kterých jsou obě rozdělené na 4 laloky. Mozková kůra: Kortex díky svému zvrásnění má rozlehlý povrch, činí asi polovinu hmotnosti mozku, na povrchu je šedá hmota a uvnitř bílá hmota. Pravá hemisféra řídí levou polovinu těla a levá hemisféra řídí pravou polovinu těla. Spolu komunikují pomocí Corpus Callosum (bílá struktura ve tvaru písmene C v centru mozku složená převážně z bílé hmoty a nervových drah).
Frontální lalok - největší lalok mozku, odpovědný za generaci volného pohybu a volné řeči. Je zde lokalizováno Brockovo centrum řeči. Přední část frontálního laloku prefrontální kůra je odpovědná za racionální procesy, rozhodování, vyhodnocování situací a vědomé předvídání (kognice), na základě toho může vybrat určitý typ chování, nebo potlačit pudové motivační úsilí pokud to sociální situace vyžaduje, je odpovědný za vymýšlení strategie -exekutivní funkce, dále se podílí na osobnostní struktuře, udržování naučených kulturních norem a morálních zákonů, reguluje emoční odpovědi. (dorzolaterální prefrontální kůra- striktně racionální “ředitel”, ventromediální prefrontální kůra - dostává informace z limbického systému o emočním stavu, kognitivní vyhodnocování emočních informací), vypíná se během REM-spánku a orgasmu. U disociální poruchy osobnosti je celkově snížená aktivita v prefrontálním kortexu.
Parietální lalok – je odpovědný za identifikaci objektů a uvědomování si prostorových vztahů, interpretuje dotek a bolest z celého těla, je zde Wernickeho řečové centrum (zasahující i do frontálního a orbitálního laloku), které slouží k porozumění mluveného jazyka.
Occipitální lalok - zadní část mozku, která vyhodnocuje zrakové informace
Temporální lalok – je odpovědný za krátkodobou a pracovní paměť, sluch (vyhodnocování řeči, hudby, rytmu), obsahuje asociační oblasti k vyhodnocování polymodálních senzorických vjemů a umožňuje rozpoznat jejich význam, a do jisté míry rozeznání čichu.
- Bazální ganglia – jsou součástí koncového mozku, jsou to šedá jádra zanořené do bílé hmoty zevně od thalamu, uplatňují se při vytváření a řízení pohybu (iniciace pohybu, regulace plynulosti), kognitivních funkcích (prostorová paměť a orientace), mají propojení s limbickým systémem, frontální a prefrontální kůrou, mozečkem… Patří sem striatum (Ncl. Caudatus, putamen), pallidum, ncl. Subthalamicus.
- ncl. accumbens- součást předního striata, patří do limbického systému - sprostředkovává kognitivní zpracování motivace, averze, odměny, pozitivního podmiňování (zásadní role ve vzniku závislosti) obsahuje dopaminergní receptory, jeho spojení s ventrální oblastní v mesencephalu (VTA) (mesolimbická dopmainergní dráha) je odpovědné za systém odměny ale i významotvornosti vjemů, má se za to, že narušením funkce - patologickou hyperaktivitou vznikají pozitivní příznaky u schizofrenie (halucinace, bludy, paranoidita).
Základy neurobiologie
Reflex - základní funkční jednotka nervové soustavy (receptor → aferentní dráha → centrum → eferentní dráha → efektor)
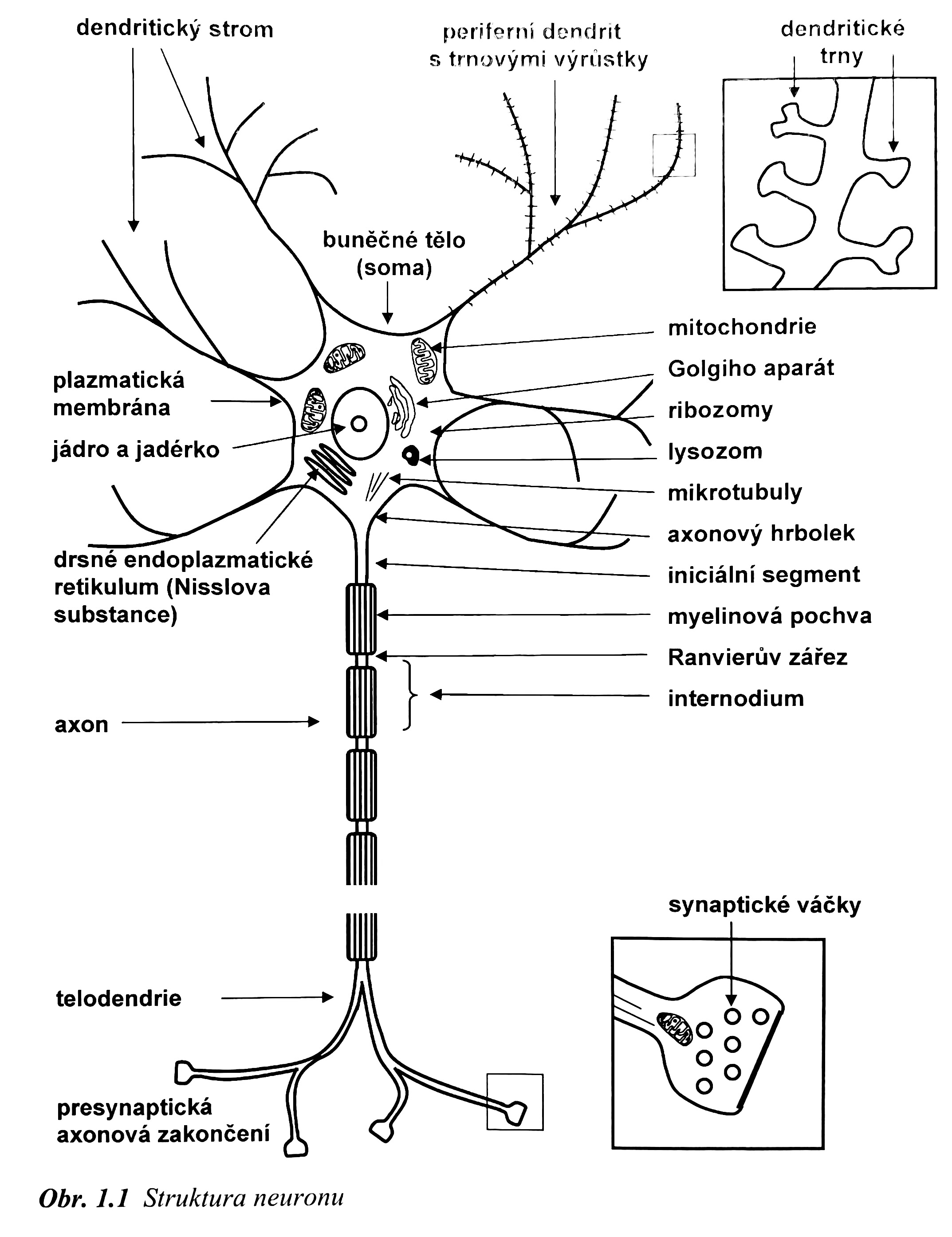
Neuron (nervová buňka) Základní morfologická jednotka centrální nervové soustavy.
Glie - pomocné buňky nervové soustavy, mají různé doplňkové funkce (metabolickou, mechanicky ochrannou, imunitní…). Například oligodendrocyty vytváří kolem axonů myelinovou pochvu, která urychluje šíření signálu.
Neurony mezi sebou přenáší informace. Přenos signálu neuronem se děje na základě změny elektrického napětí na membráně neuronu - membránový potenciál.
Klidový membránový potenciál – Vnitřek membrány je v klidu negativně elektricky nabitý oproti okolí díky rozdílné koncentraci elektricky nabitých iontů na obou stranách membrány: tento stav se nazývá “polarizace” v základním stavu je kolem –70mV.
Elektrické napětí na semipermeabilní (polopropustné) cytoplasmatické membráně neuronu je v klidovém stavu udržované proteinovou konstrukcí vnořenou do membrány – Na K ATPáza- sodnodraselná iontová pumpa (přesouvá za 1 molekulu ATP 3 ionty sodíku ven a 2 ionty draslíku dovnitř neuronu). Na svoje fungování potřebuje velké množství energie.
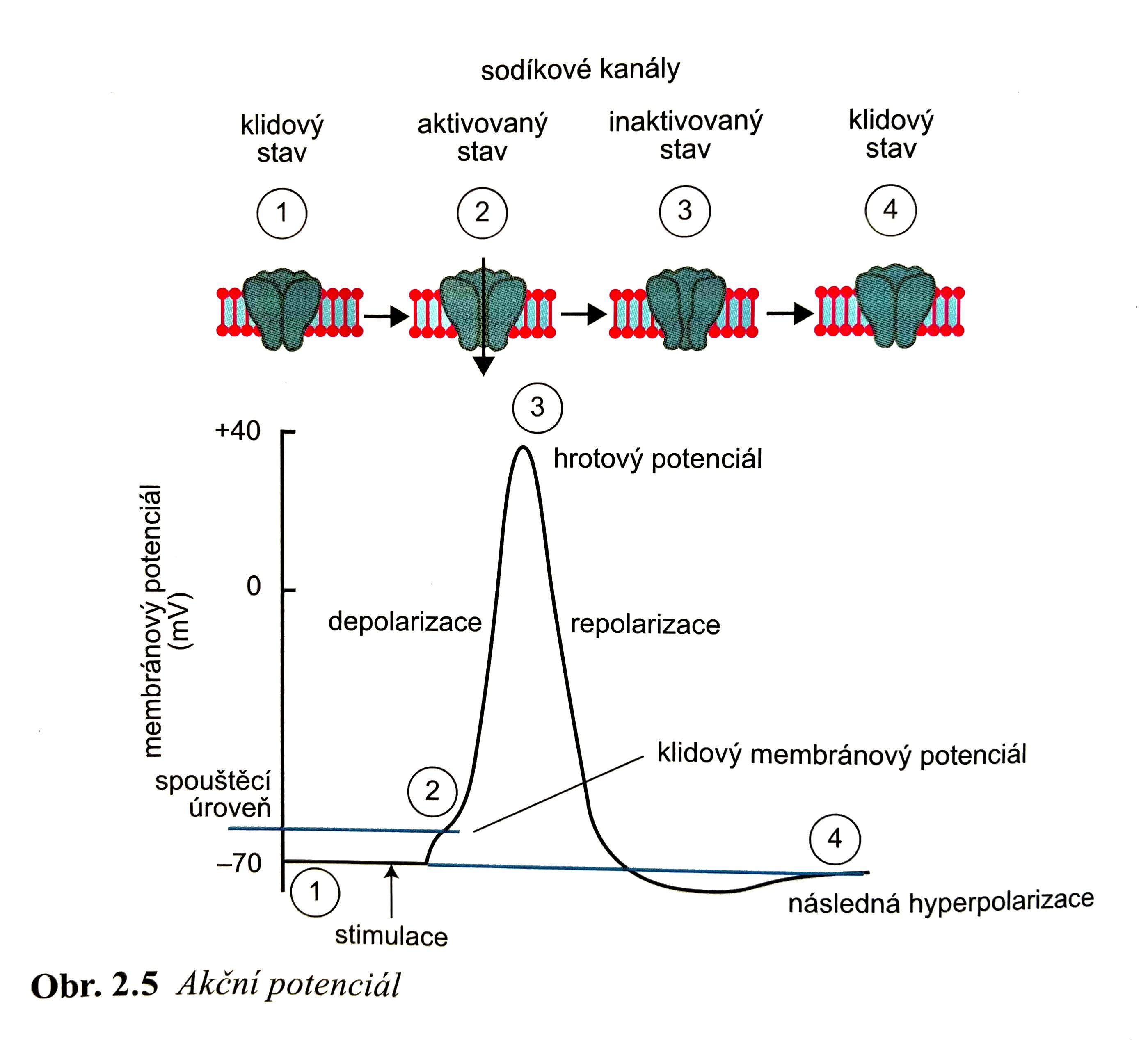
Akční potenciál - depolarizace membrány (změna z negativního náboje na pozitivní) se šíří od těla neuronu po axonu k synaptickému zakončení.
V těle neuronu se kumuluje součet elektrických signálů přijatých od jiných neuronů cestou dendritů. Tyto signály jsou buď excitační (depolarizující membránu- měnící membránový potenciál na kladnější), nebo inhibiční (hyperpolarizující membránu- měnící membránový potenciál na ještě více záporný).
Pokud převyšuje signál excitační a je dostatečně intenzivní (tzv. generátorový potenciál) v iniciálním segmentu axonu, který se nachází těsně před prvním myelinovým segmentem vzniká akční potenciál (Jakmile depolarizace membrány dosáhne určitého bodu- ca -55mV, otevřou se sodíkové kanály, které dále stimulují depolarizaci influxem iontů sodíku dovnitř membrány). To spouští kaskádu depolarizace a membránový potenciál se na chvíli mění na pozitivní.
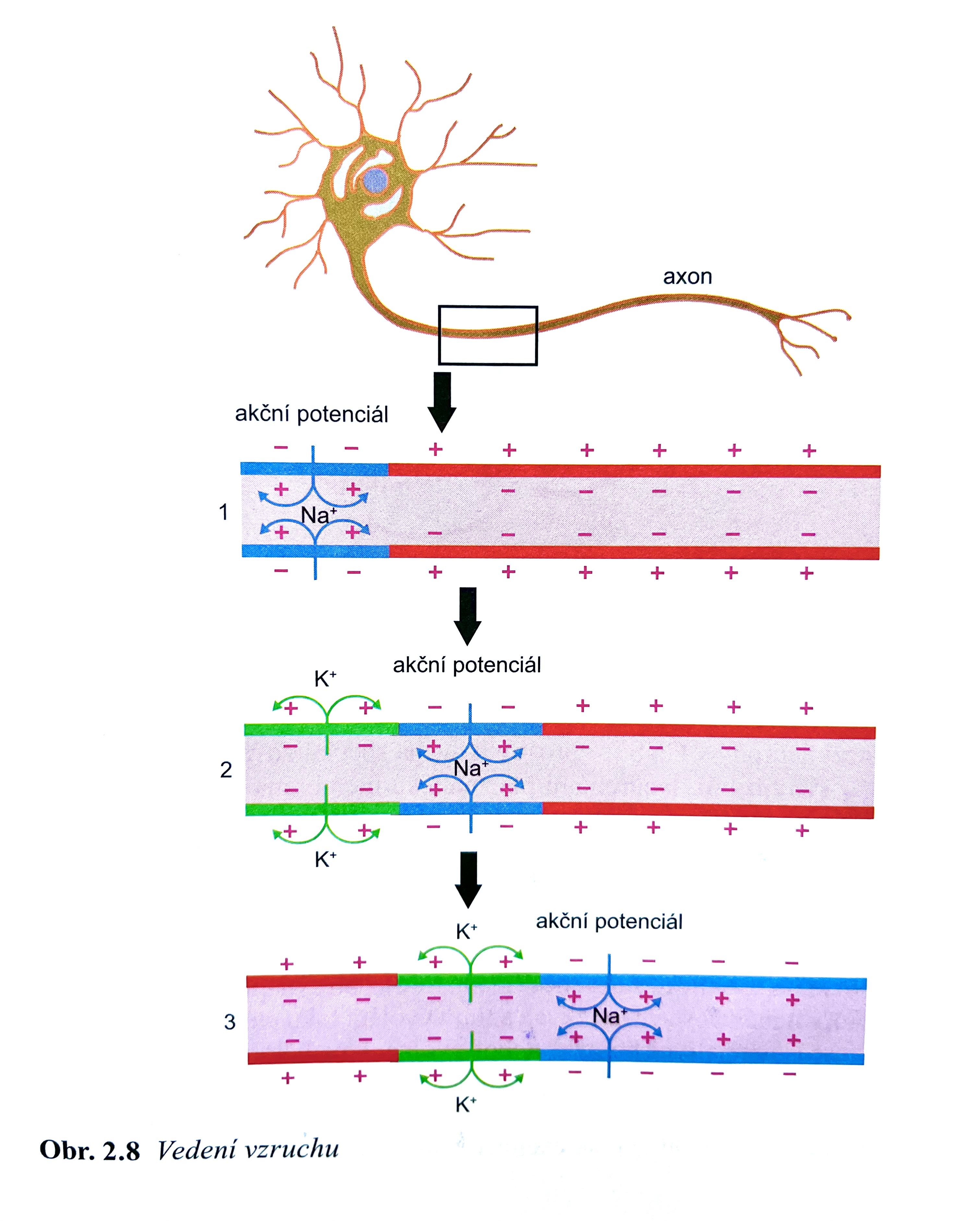
Vzhledem k tomu, že právě depolarizovaná membrána zůstává nějaký čas refrakterní (nelze opět depolarizovat) šíří se vzruch vždy pouze jedním směrem od iniciálního segmentu u těla neuronu po axonu k terminálnímu synaptickému zakončení.
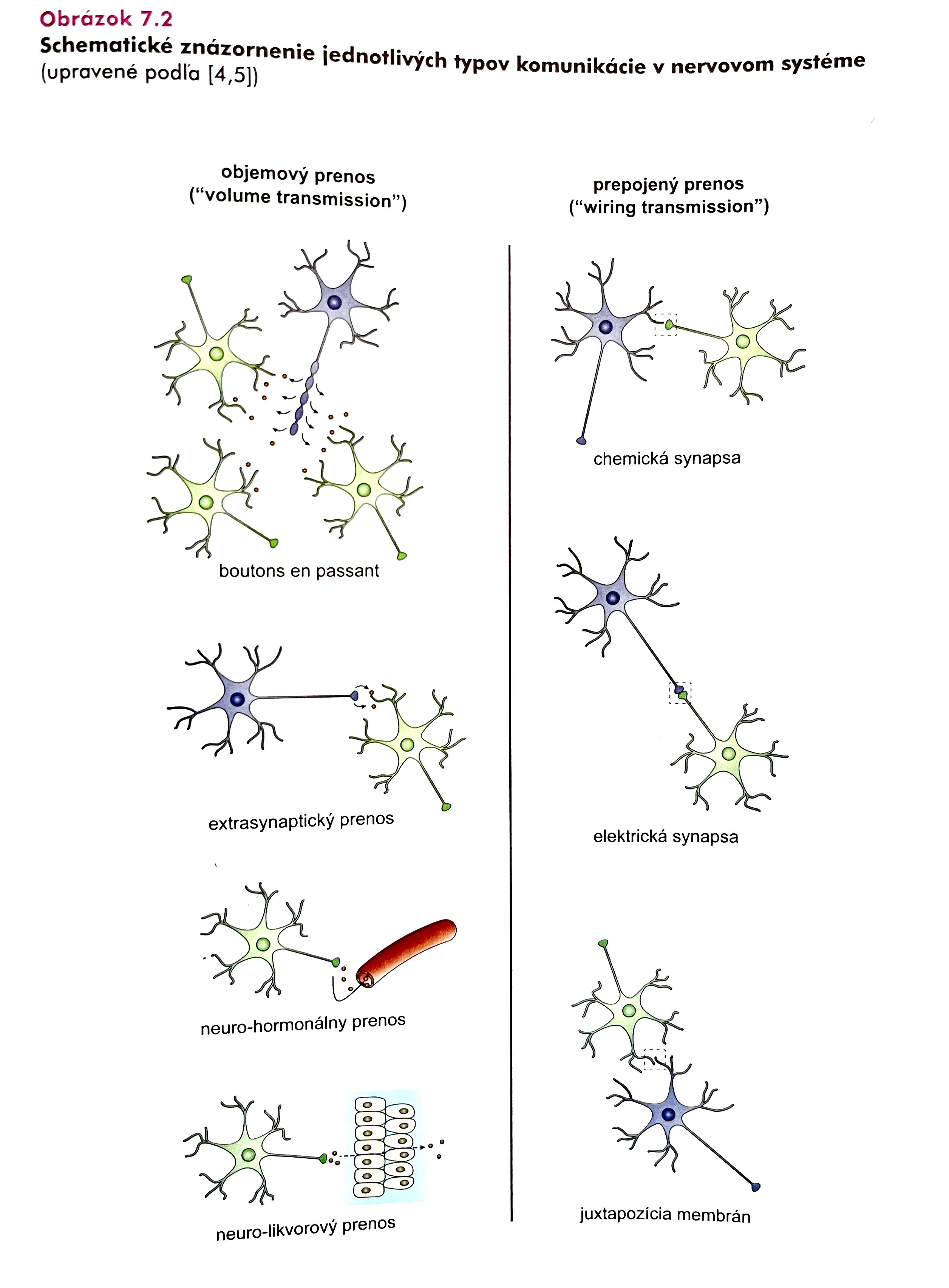
Neurotransmise – přenos signálu mezi jednotlivými neurony Signál se šíří buď prostřednictvím propojení mezi neurony – synapse může být buď chemická – zprostředkována chemickými látkami neurotransmitery (neuropřenašeči), které jsou vyráběné a skladované v neuronech a uvolňované z axonových zakončení., nebo elektrická- zprostředkovaná tight junctions mezi membránami dvou neuronů. Dále se signál může šířit objemovým přenosem, když se uvolní neurotransmiter z axonového zakončení mimo synaptickou štěrbinu a má tak dosah na větší počet okolitých neuronů.
Chemická synapse
Složení:
- Presynaptická část (synaptické zakončení termínálních větví axonu prvního neuronu). Produkuje, uvolňuje a zpětně vychytává neurotransmiter. Neurotransmiter je v synaptických zakončeních skladován ve váčcích (vezikulách)
- Synaptická štěrbina- do ní se uvolňuje neurotransmiter z presynaptické části (může obsahovat enzym rozkládající neurotransmiter)
- Postsynaptická část (spravidla dendrit druhého neuronu) - obsahuje receptory pro daný neurotransmiter
Receptory jsou proteinové konstrukce vnořené do membrány, které po své aktivaci můžou provádět změny na membráně nebo v buňce. Svou stavbou jsou specificky citlivé. Jen určitý typ molekuly se může na jejich povrch navázat a aktivovat je. Receptory v nervovém systému reagují na neurotransmitery a neuromodulátory. (dělíme je podle toho na serotoninové, dopaminové etc.)
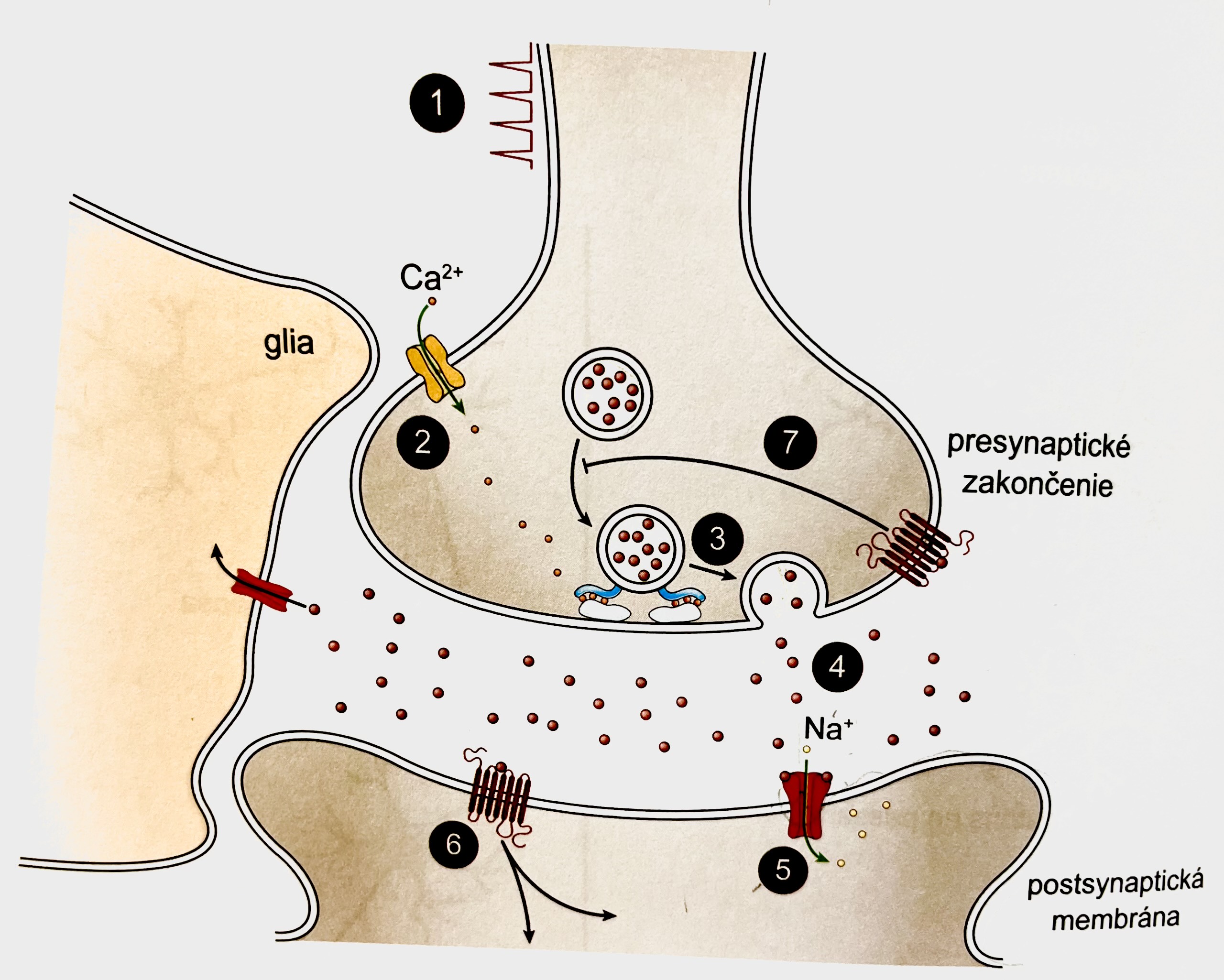
Synaptický přenos
Akční potenciál doputuje k synaptickému zakončení (1), kde se nachází napěťově řízené iontové kanály pro ionty vápníku, ty se působením membránové depolarizace aktivují (2), způsobí proudění vápníku dovnitř buňky a v důsledku toho splynutí vezikul s membránou (3) a vylití neurotransmiteru do synaptické štěrbiny (4).
Účinky neurotransmiteru po jeho vylití:
- Na postsynaptické membráně (membrána druhého neuronu) : navázání na receptory (podle typu receptoru)
- Ionotropní (chemicky řízené iontové kanály) (5)
- zprostředkují efekt na membráně - jejich aktivací dochází k jejich otevření/ uzavření a přesunu iontů přes membránu - v důsledku toho excitace/inhibice dalšího vedení signálu neuronem.
- Metabotropní (modulační) (6)
- regulují děje uvnitř buňky - zasahují do metabolismu neuronu, důsledky jejich působení trvají dny až měsíce, podílí se na strukturálních a funkčních změnách na synapsích. zodpovídají např. za výsledný stupeň reaktivity nervového systému, mají význam např. na emoční reaktivitě a regulaci (bývají cílem farmakoterapie)
- změny genové exprese druhého neuronu (syntéza nových proteinů, receptorů)
- trofické změny (ovlivňování růstu nových zakončení, migrace, diferenciace, maturace synáps a zánik buněk)
- můžou také působit zevnitř buňky na otevření okolitých iontových kanálů a regulovat i membránový potenciál a vedení vzruchu
- Na presynaptické membráně
- navázání na autoreceptory (7) inhibuje vylití dalšího neurotransmiteru do synaptické štěrbiny, princip zpětnovazebné regulace množství receptoru v synaptické štěrbině aby se zabránilo delšímu přetrvávání signálu, než je potřeba.
Další osud neurotransmiteru po vylití
- Neurotransmiter je vstřebán zpátky do vezikul presynaptického zakončení prvního neuronu k dalšímu použití později. Tzv. REUPTAKE Slouží k němu transportéry (SERT pro serotonin, DAT pro dopamin, NET pro noradrenalin a dopamin), jejich blokáda bývá cílem farmakoterapie - zvyšuje dostupnost neurotransmiterů v synaptické štěrbině a tím intenzitu jejich působení na receptory.
- Neurotransmiter je rozložen pomocí enzymu přítomného buď v synaptické štěrbině, nebo v buňkách přítomné neuroglie a produkty rozkladu můžou být transportovány zpátky do neuronu kde slouží jako substráty k syntéze nového neurotransmiteru.
enzymy, kterých inhibice bývá cílem farmakoterapie:
- Monoaminooxidáza: MAO pro serotonin, dopamin, noradrenalin
- Katechol-O-methyltransferáza: COMT pro dopamin, noradrenalin
- Acetylcholinesteráza pro acetylcholin
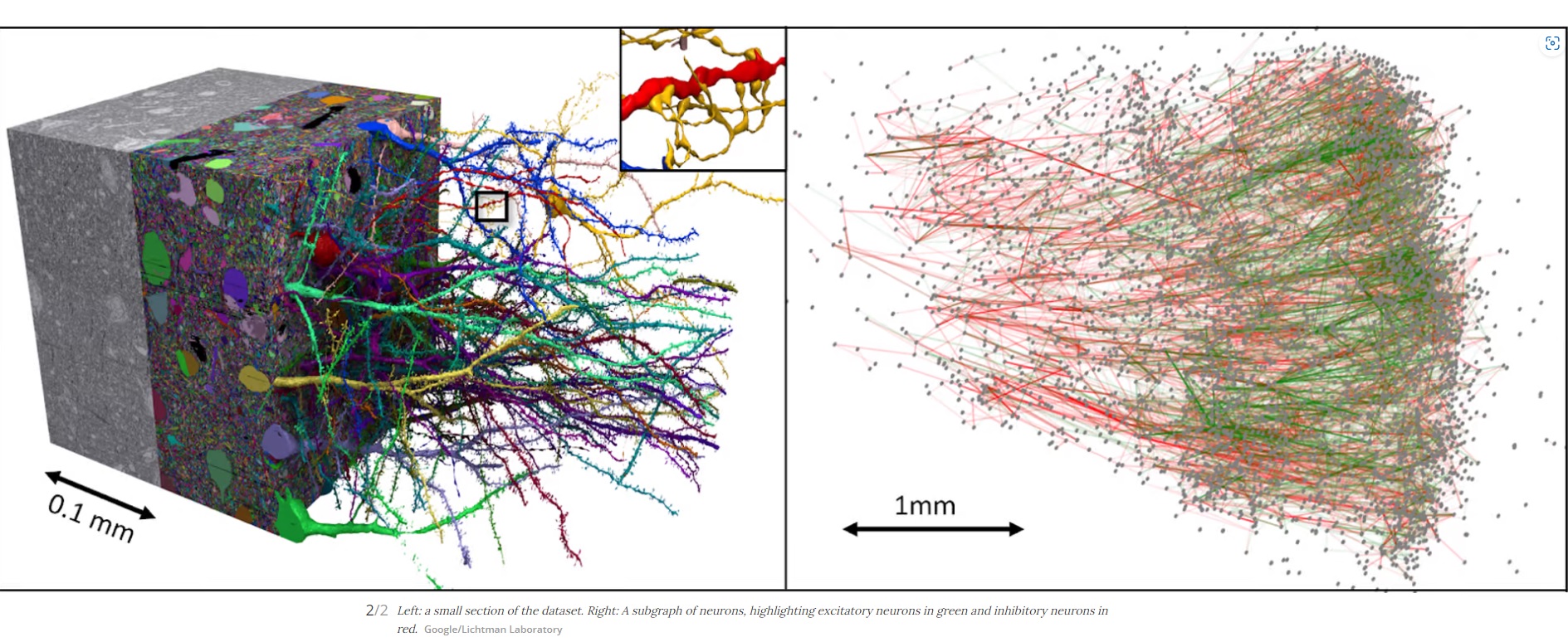
Konektom (propojení jednotlivých nervových drah v mozku):
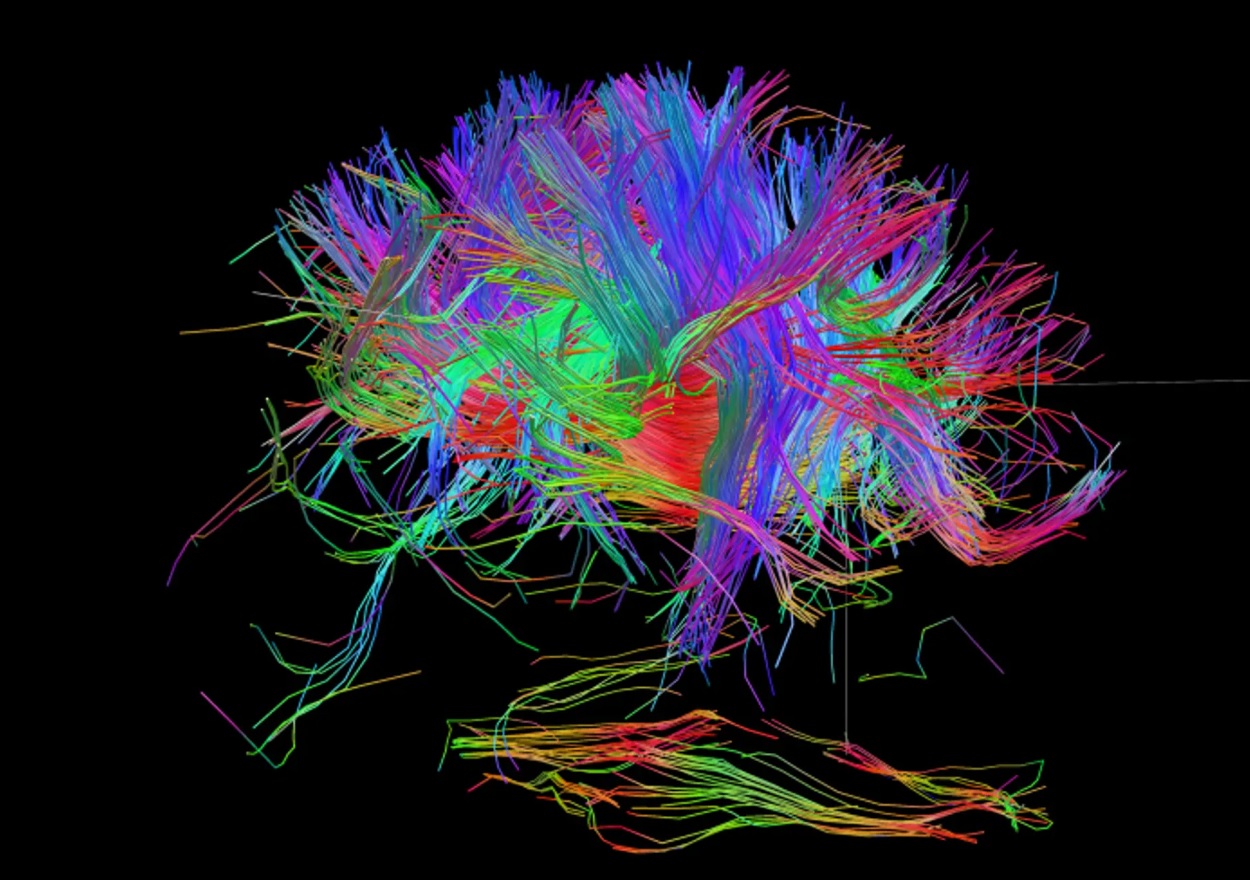
V 1 mm3 mozkové tkáně (který se povedlo zmapovat pomocí elektronového mikroskopu) je kolem 57,000 neuronů a asi 150 milionů synapsí (mapování 1 mm kubického mozkové tkáně vygenerovalo 1,4 milionu GB dat) V celém mozku je asi 86 miliard neuronů a asi 150 trilionů synapsí. zdroj
Synapse v elektronovém mikroskopu i s vezikulárními váčky:
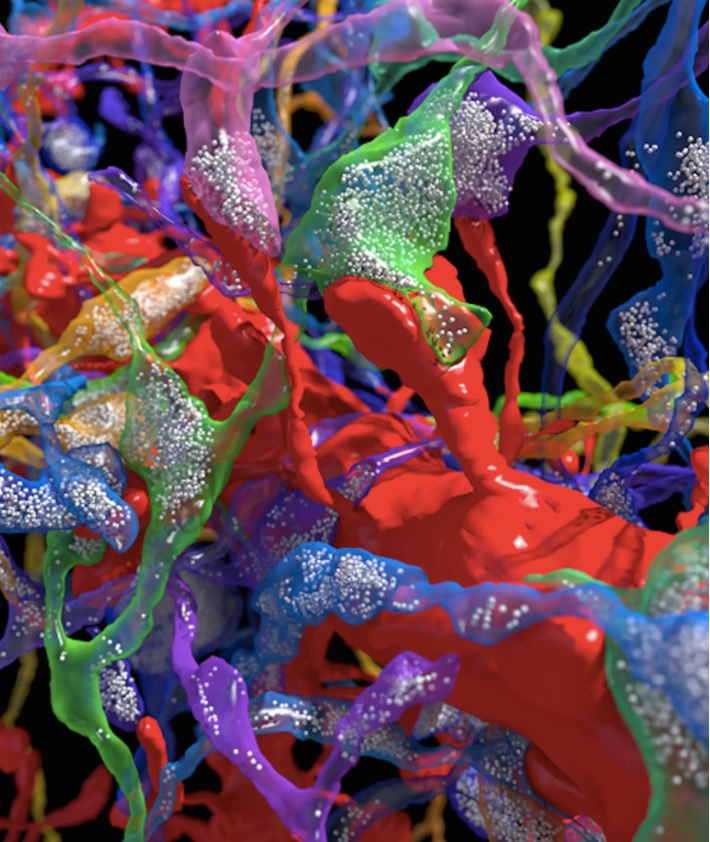
Systémy neurotransmiterů
-neuromediátor (přenos elektrického signálu přes ionotropní receptory), zejména glutamát, GABA
-neuromodulátor (šíření signálu přes metabotropní receptory) ostatní neurotransmitery.
- Aminokyseliny (podílí se zejména na zesilování a zeslabování vedení signálu mezi neurony - aktivaci nebo útlumu mozkové činnosti)
- Excitační - Glutamát - Glu
- Inhibiční - kyselina gama-amino-máselná - GABA
- ostatní neurotransmitery mají specifičtější funkce spojené mimo jiné s mentální aktivitou:
- Acetylcholin - ACh
- Monoaminy
- Dopamin - D
- Noradrenalin - NA
- Serotonin - (5-hydroxytryptamin) 5-HT
- Histamin - H
- Opioidy
- Další: neuropeptidy, plynné neurotransmitery, neurosteroidy…
Změny hladin neurotransmiterů hrají roli v patogenezi duševních onemocnění a jsou cílem farmakoterapie. V patogenezi duševních poruch se nejedná pouze o snížení nebo zvýšení neurotransmiteru, záleží i na místu změny jeho hladiny. Uplatňují se i změny receptorů pro daný mediátor: hustota receptorů v daném místě, reaktivita receptorů (závislá např. na genetické variabilitě, přítomnosti inhibitorů/kompetitorů) etc. Neurální dráhy jednotlivých mediátorů se vzájemně ovlivňují a propojují do složitých funkčních systémů. Existuje mnoho podtypů receptorů pro jednotlivé neurotransmitery, které mají různé působení v různých oblastech mozku. Ovlivnění jedné dráhy má důsledky v ovlivnění ostatních drah.
Aminokyseliny
Glutamát
- funkce: excitace neuronových membrán, facilitace nesení signálu, přenášení senzorických informací, učení, paměť, pohyb, regulace emocí, kognice.
- zvýšení - excitotoxicita (excesivní stimulace receptorů při extrémním zvýšení transmiteru a v důsledku toho omezení propojení až zánik neuronů), epilepsie
- snížení - nerovnováha se projevuje u řady duševních poruch (schizofrenie, BAP…)
- receptory - Ionotropní (NMDA, AMPA, kainát), Metabotropní (mGlu)
- ovlivnění - blok NMDA: Memantin, Lamotrigin, Ketamin, PCP, Mg, Zn
- lokalizace - většina neuronů CNS na všech úrovních
GABA
- funkce - inhibice neurotransmise, celkové klidnění
- zvýšení - zklidnění, útlum, spánek, myorelaxace
- snížení - epilpesie, úzkost, dyskineze (poruchy pohybů), nespavost, dysforie, neklid
- receptory - Ionotropní (GABA-A, GABA-B) Metabotropní (GABA-C)
- ovlivnění - GABAA aktivace: alkohol, Benzodiazepiny, Barbituráty, Z- hypnotika, antiepileptika, Blok: flumazenil
- lokalizace - interneurony kůry a podkorových funkčních okruhů (bazáklní ganglia, mozeček)
Acetylcholin
- funkce- bdění, kognice, paměť, učení, motivace, lucidita vědomí
- zvýšení - Zvýšení kognice, soustředění, (Lucidní sny)
- snížení - chronicky: demence, akutně: dezorientace, delirium
- receptory - Ionotropní (Nikotinové) Metabotropní, (Muskarinové: M1-5)
- ovlivnění - Blok M: NÚ psychofarmak, delirogeny, Aktivace nAch: nikotin
- * lokalizace - ncl. basalis Meynerti, Septum verum, kůra, basální ganglia, pons, eferentní neurony, parasympatikus
Monoaminy
Dopamin
- funkce- motivace, systém odměňování, soustředění, konsolidace paměti, regulace pohybu, hormonální regulace
- zvýšení - zvýšení iniciativy, asertivity, psychóza (bludy, halucinace, paranoia), chorea (neregulované mimovolné pohyby)
- snížení - apatie, abulie, anhedonie, snížení apetence (sex, jídlo), hypoprosexie, M. Pakrinson, hyperprolaktinemie
- receptory - Metabotropní (D1-5)
- ovlivnění - Aktivace: Antiparkinsonika, amfetaminy, kokain, methylfenidát, Blok: Antipsychotika
- lokalizace- Substantia nigra, Ventrální tegmentální oblast (area ventralis tegmenti Tsai- VTA)
4 dopaminergní dráhy (s významem pro psychopatologii a farmakologii):
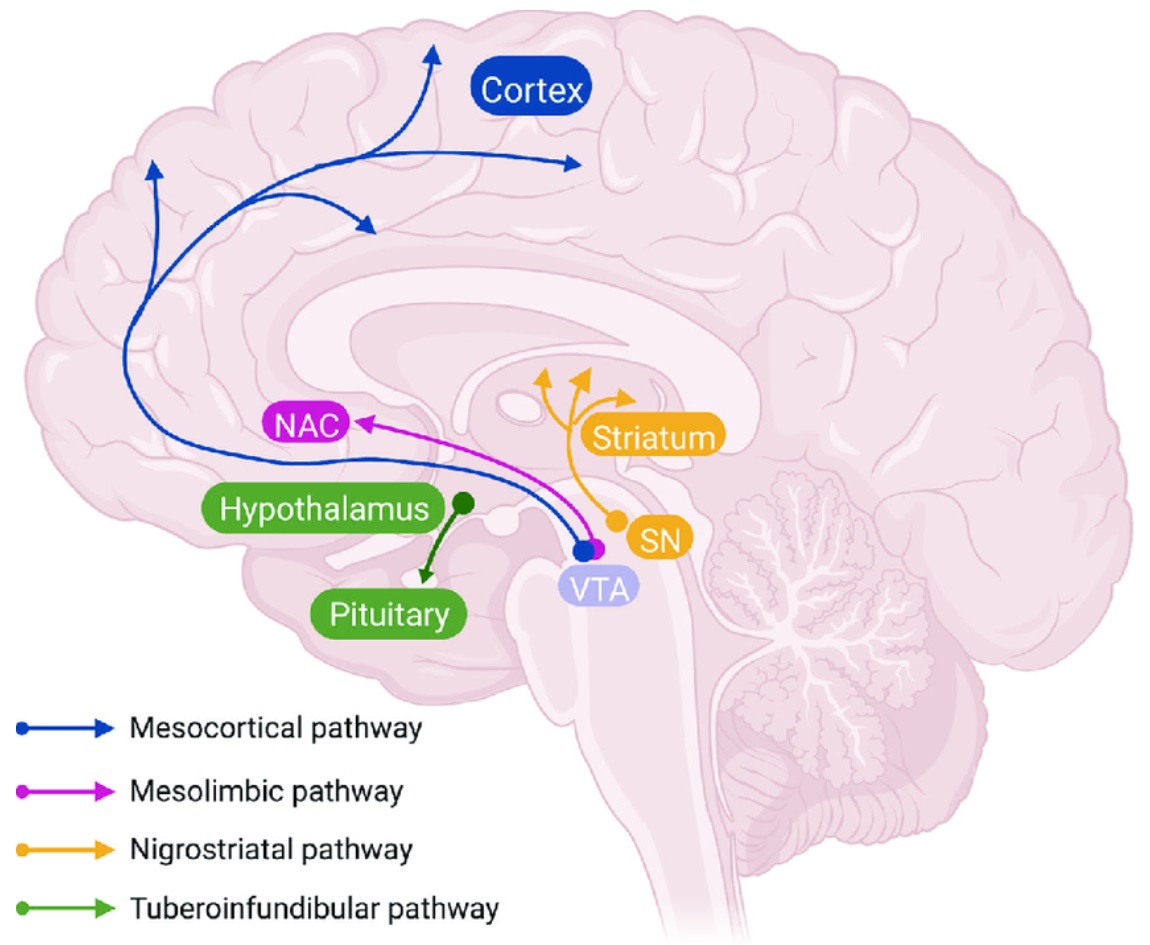 zdroj obrázku
zdroj obrázku
- mesolimbická - od Ventrální tegmentální oblasti (VTA) k nucleus accumbens (NACC)
- systém odměny - habituace na intenzivní podněty zde vede ke vzniku závislosti,
- systém připisování významu okolním podnětům - narušení funkce vede k neschopnosti správně vyhodnotit význam podnětů a má se za to, že zvýšená dopaminergní signalizace zde souvisí s paranoidními prožitky u psychóz (a tzv. pozitivní příznaky u SCH- bludy, halucinace).
- mesokortikální - od Ventrální tegmentální oblasti (VTA) k frontální mozkové kůře (Cortex)- vede k aktivizaci, má vliv na kognitinvní funkce, na emoce, kontrolu chování a impulzivitu. Nedostatek dopaminu v této oblasti vede k depresivním a pseudodementním příznakům (rovněž i k negativním schizofrenním příznakům- apatie, abulie, anhedonie, porucha exekutivních funkcí). Tato transmise je blokovaná neurony se serotoninergními 5-HT2 receptory. Blok těchto 5HT-2 receptorů zvyšuje dopaminergní signalizaci v kortexu (mechanizmus působení některých modernějších antipsychotik a antidepresiv).
- nigrostriatální - od substantia nigra (SN) k bazálním gangliím (Striatum)- řídí plynulost pohybu - nedostatek dopaminu v této dráze vede k parkinsonickým příznakům (třes končetin, psychomotorické zpomalení, deprese, hypomimie, svalová rigidita), častý nežádoucí účinek farmakoterapie antipsychotiky.
- tuberoinfundibulární - z hypothalamu do hypofýzy - dopamin zde inhibuje vylučování prolaktinu. nedostatek dopaminu v této dráze má za následek hyperprolaktinémii (častý nežádoucí účinek farmakoterapie antipsychotiky).
Noradernalin
- funkce - bdění, paměť, stres, nabuzení, regulace vnímání bolesti
- zvýšení - nabuzení, zvýšení PMT, tenze, úzkost
- snížení - hypoprosexie, únava, apatie, anhedonie, nevýkonnost
- receptory - metabotropní ( α 1A-D, 2A-D, β 1-3)
- ovlivnění - farmakologické ovlivnění noradrenergního systému zejména přes NET
- lokalizace- locus coeruleus, retikulární formace, regulační interneurony
Serotonin- 5- hydrpxytryptamín
- funkce - neurotrofní procesy (regulace růstu nových synaptických zakončení, maturace neuronů, dělení buněk) celková modulace a vylaďování mozkové signalizace, regulace nálady, snižování impulzivity a emoční reaktivity na stresové podněty, regulace cirkadiánních rytmů, spánku a bdění, příjmu potravy, sexu, má další funkce v těle (GIT, KVS etc.)
- zvýšení - serotoninový syndrom, napětí, tenze, třes
- snížení - úzkost, iritabilita, hostilita, impulzivita, agitovanost, hypochondrie, suicidalita, agresivita
- receptory - Ionotropní (5-HT 3) Metabotropní (5-HT 1-8), ještě dělení jednotlivých receptorů na A,B,C… Má asi 17 podytpů receptorů v mozku, které mají různou funkci na různých místech.
- ovlivnění - Blok SERT: SSRI, Aktivace receptorů: DMT, LSD, MDMA, psilocybin, multimodální antidepresiva
- lokalizace - ncl. raphe a z něj příslušné nervové dráhy do všech úrovní CNS.
Histamin
- funkce- regulace spánek- bdění, energetická a endokrinní homeostáza, příjem potravy, neuroplasticita
- zvýšení - hyperaktivace, nespavost, úzkost, tenze
- snížení - útlum, únava, nesoustředění, zvyšování hmotnosti
- receptory - Metabotropní (H1-4)
- ovlivnění - Blok: některé antidepresiva, antipsychotika a anxiolytika
- lokalizace - ncl. tuberomammilaris hypothalamu- dráhy do všech oblastí CNS
Opioidy
- funkce- regulace vnímání bolesti, příjmu potravy, činnosti KVS, inhibice motility GIT, zprostředkování libých pocitů
- zvýšení - euforie, slast, útlum dechového centra, zpomalení střevních pohybů, snížená apetence (sex, jídlo)
- snížení - dysforie, zvýšení vnímání bolesti, anhedonie
- receptory - Metabotropní (µ , δ , κ)
- ovlivnění - Aktivace: Heroin, Morfin, Kodein, Oxykodon, Fentanyl, buprenorfin,loperamid… etc., blok: Naltrexon, Naloxon , Parciální agonismis: Nalmefen
- lokalizace - limbický systém, hypothalamus, mozkový kmen, mícha
Neuroplasticita
Schopnost mozku měnit se v průběhu života vlivem faktorů prostředí a získaných zkušeností. Zejména se jedná o celoživotní schopnost neuronů vytvářet nové synapse, co vede k vytváření a udržování nových drah a spojení, nebo opouštění starých drah (slábnutí signálu při nepoužívání) co má za následek přepisování starých naučených vzorců chování a přemýšlení novými.
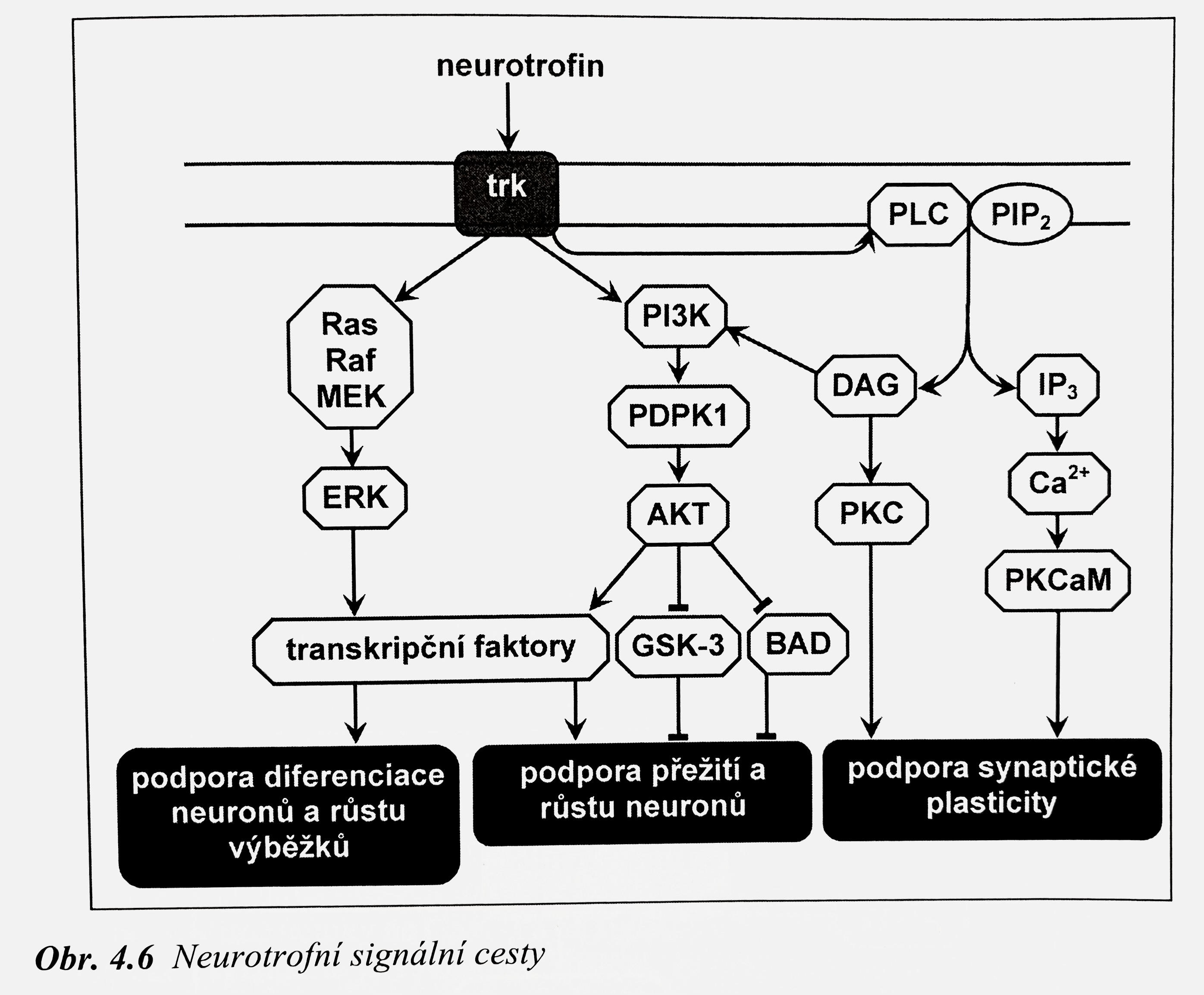
Na molekulární úrovni je základní faktor neuroplasticity BDNF (brain derived neurotrophic factor) protein působící jako růstový faktor nervové tkáně. Stimuluje růst nových dendritických trnů (výběžky dendritů připravené přijmout signál- postsynaptické části synapsí), má vliv na udržování dlouhodobé paměti, jeho exprese reaguje na vnější vlivy.
Úroveň neuroplasticity můžeme makroskopicky sledovat na objemu mozkových struktur, u řady duševních onemocnění byl pozorován úbytek mozkové hmoty v jednotlivých mozkových strukturách a snížená úroveň neuroplasticity (snížení hladin BDNF).
Např. U deprese je patrný snížený objem prefrontálního kortexu, hippokampu, striata a zvětšení 3. komory. (tyto změny jsou reverzibilní léčbou antidepresivy).
U Schizofrenie je nižší hustota neuronů a objem hippokampu, úbytek šedé hmoty v temporálním spodní frontální a bilaterálně v cingulární kůře. Tato redukce tloušťky je především v důsledku redukce dendritických trnů.
U PTSD se zvyšuje celkový objem amygdaly.
Faktory vedoucí k zániku propojení, nebo celých neuronů:
- toxiny vnější a vnitřní, excitotoxicita (excesivní stimulace receptorů při extrémním zvýšení transmiteru), chronický stres, degenerativní onemocnění, nedostatek stimulace, chronický zánět, působení oxidativního stresu
Faktory podporující neurogenezi:
fyzický pohyb, meditace, psychoterapie, léčba antidepresivy, Lithiem, VLP, ketamin, psilocybin, elektrokonvulzivní terapie…
Zjednodušeně platí, že mozek funguje podobně jako sval: oblasti a dráhy, které jsou aktivně používané, rostou. Při nepoužívání nebo poškození atrofují.
Genetické faktory
Dědičnost v psychiatrii je spřažená: některé geny hrají roli u více diagnóz (SCH + BAP + unipolární deprese), genetické poznatky tedy nekorespondují s aktuální klasifikací, zatím je také nemůžeme příliš využít v praxi.
V etiologii téměř žádné duševní poruchy nehraje roli pouze 1 gen. Vždy se jedná o více genů, přičemž význam jednoho genu je velmi malý - polygenní dědičnost.
Jedná se o variability genů kódujících:
- enzymy syntézy neurotransmiterů
- neurotransmitery
- receptory
- transportéry
- regulaci buněčné fyziologie
- produkci BDNF a další faktory neuroplasticity
- mitochondriální funkce
- atd…
Monogenně podmíněná duševní porucha je například Huntingtonova choroba (Autozomálně dominantní dědičná porucha s expanzí tripletu CAG v genu pro huntingtin na 4. chromozomu, Mentální retardace u Downova syndromu (trizomie 21. chromozomu)
Dnes se zkoumají CNVs (copy number variations) - rozsáhlejší strukturální abnormity DNA: delece nebo duplikace nukleotidových bází (1000 a více), co vede k chybění nebo nadprodukci určitého proteinu, což následně interferuje s činností neuronů. Bývají vzácné, ale mají velkou penetraci. Geny takto postižené mají vztah k neuroplasticitě, ke glutamátergní transmisi (podíl např, u SCH, u autismu, u MR). Můžou být zděděné, ale i vzniklé nově při buněčném dělení.
U většiny duševních poruch předpokládáme určitou míru dědičnosti. Podíl genetických faktorů na přítomnost duševního onemocnění odráží Index heritability (vypočítán genealogickými studiemi a studiemi dvojčat) Zbytek je dán vnějšími faktory.
- Demence 0,4-0,7
- Závislost na návykových látkách 0,4-0,6
- Schizofrenie 0,6-0,8
- Poruchy nálady 0,4-0,6
- Neurotické a úzkostné poruchy 0,2-0,4
- Mentální anorexie 0,5-0,7
- Poruchy osobnosti 0,3-0,5
- Mentální retardace 0,7-0,8
Epigenetika
Zkoumá změny v genové expresi, které nejsou způsobené změnou nukleotidové sekvence DNA, ale aktivací, nebo deaktivací určitého genu působením vnějších faktorů (methylace, alkylace na histonech) (nevyhýbá se ani spermiím a vajíčkům, tyto změny jsou přenositelné do dalších generací).
STRES a traumatizace
Stres je v širším pojetí nespecifická odpověď organismu na požadavek po změně. Na biologické úrovni se jedná se o kaskádu dějů, které mají mobilizovat energetické zdroje a organizmus připravit na vypořádání se se stresorem (tím, co stres vyvolalo). Stresová reakce může mít aktivizační a motivační funkci a je jednoznačně výhodná v boji o biologické přežití (evolučním cílem je přežít, nikoliv cítit se dobře). Jeho účinnost je ale pochybná, pokud se spouští v reakci na (někdy i malicherní) podněty z psychosociální oblasti, které můžou být vnímány jako ohrožující.
Stresory se dají rozdělit na fyzikální, tělesné, chemické a psychosociální. Stresory přicházející z psychosociální oblasti mají na organizmus stejný vliv jako stresory biologické, jsou považovány za významný faktor ve vzniku deprese. Rovněž se používají jako jedna z hlavních experimentálních cest k depresivnímu chování u laboratorních zvířat.
Odpověď organizmu na stresor je regulovaná v CNS a na periferii zprostředkovaná autonomním vegetativním nervovým systémem.
Na úrovni CNS se na regulaci podílí amygdala, thalamus, hypokampus a prefrontální kortex. Ve stavu nabuzení spolu interaguji dva základní systémy:
1. “HOT” systém: (poplašený systém, “alarm”)- ve stavu ohrožení se aktivuje amygdala, která následně vede přes aktivaci locus coeruleus (noradrenergní jádro) a hypothalamu ke zvýšení tonu sympatiku (spuštění stresových os):
- sympato-adreno-medulární - rychlá, vede k vylučování katecholaminů (adrenalin, noradrenalin) rychlé mobilizaci energie, zvyšuje napětí a prokrvení svalů, zvyšuje bdělost a nabuzení, zvyšuje se krevní zásobení kosterního svalstva a snižuje se zásobení gastrointestinálního systému funkce nepotřebných systémů - GIT, urogenitální systém atp.
- hypothalamo-hypofýzo-adrenální (HPA osa)- pomalá, vede k zvýšenému výdeji glukokortikoidů (kortizolu) z kůry nadledvinek, cílem je mobilizace další energie k překonání/přečkání nepříznivé situace. HPA osa má velký vliv na náladu a motivaci, protože velmi blízce interaguje s limbickým systémem.
Kortizol má širokospektré účinky: katabolismus, zvyšování glykemie, zvyšování periferní inzulinové rezistence, potlačuje imunitní odpověď a blokuje sexuální chování a růst, zpětnovazebně inhibuje aktivitu hypothalamu a hypofýzy k vyhasnutí stresové odpovědi. Ve zvýšených koncentracích působí neurotoxicky (inhibuje neurogenezi, snižuje BDNF, zvyšuje aktivaci a excitotoxicitu glutamátu)
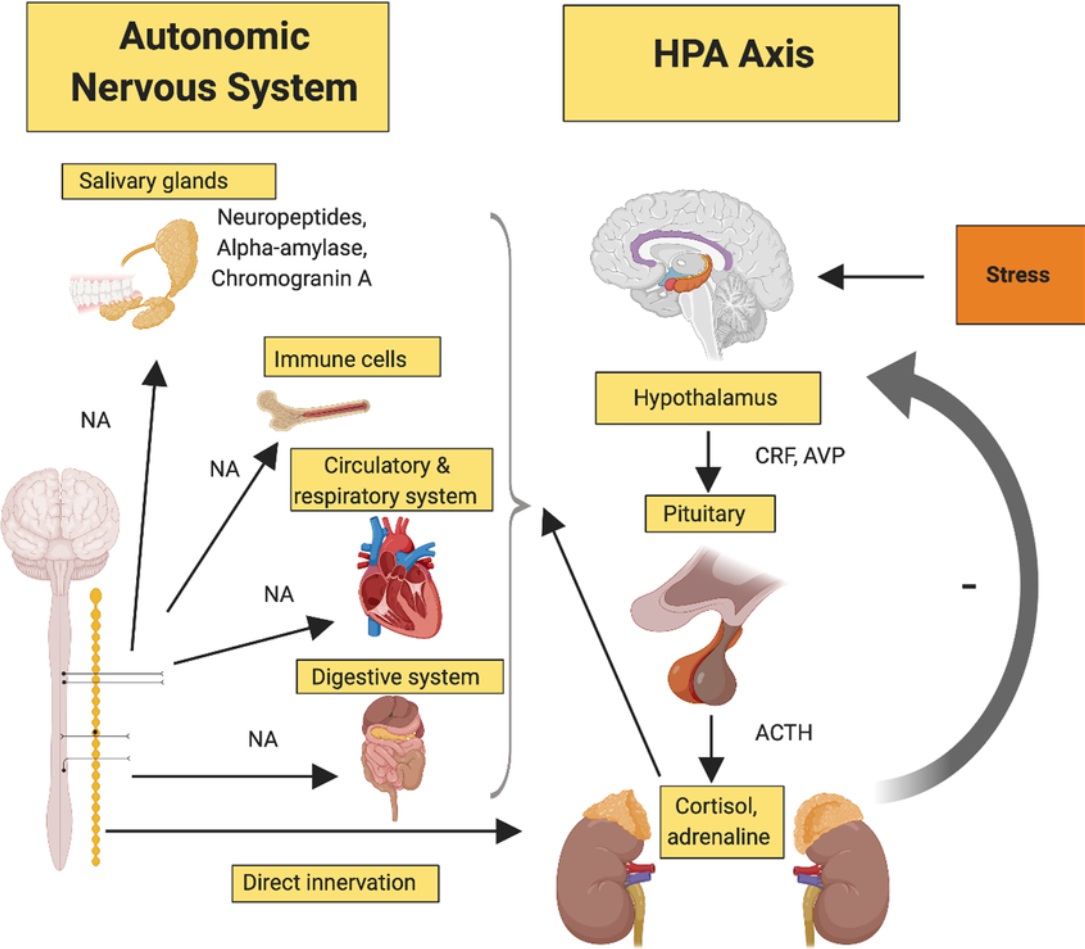
2.”COOL” systém - zprostředkován hipokampem, thalamem a prefrontální kůrou. Hipokampus má významný inhibiční vliv na HPA osu a obsahuje velké množství glukokortikoidních receptorů. Zprostředkovává racionální vyhodnocení situace (propojení s prefrontální kůrou) a porovnání s minulými událostmi, má přístup k archivu naší paměti, má propojení s mozkovými hemisférami a s thalamem, kde probíhá integrace jednotlivých částí stresové odpovědi (racionální a emoční část). Má výrazný vliv na tlumení a mírnění poplašné reakce.
Sympatikus v absenci ohrožení zprostředkovává motivační aktivitu. V přítomnosti ohrožení poplachovou reakci přípravy organizmu na útok- boj s ohrožením nebo útěk (fight/flight response).
Antagonisticky proti němu působí Parasympatikus (přední větev) odpovědný za pochody během klidu (trávení, relaxace, šetření energie).
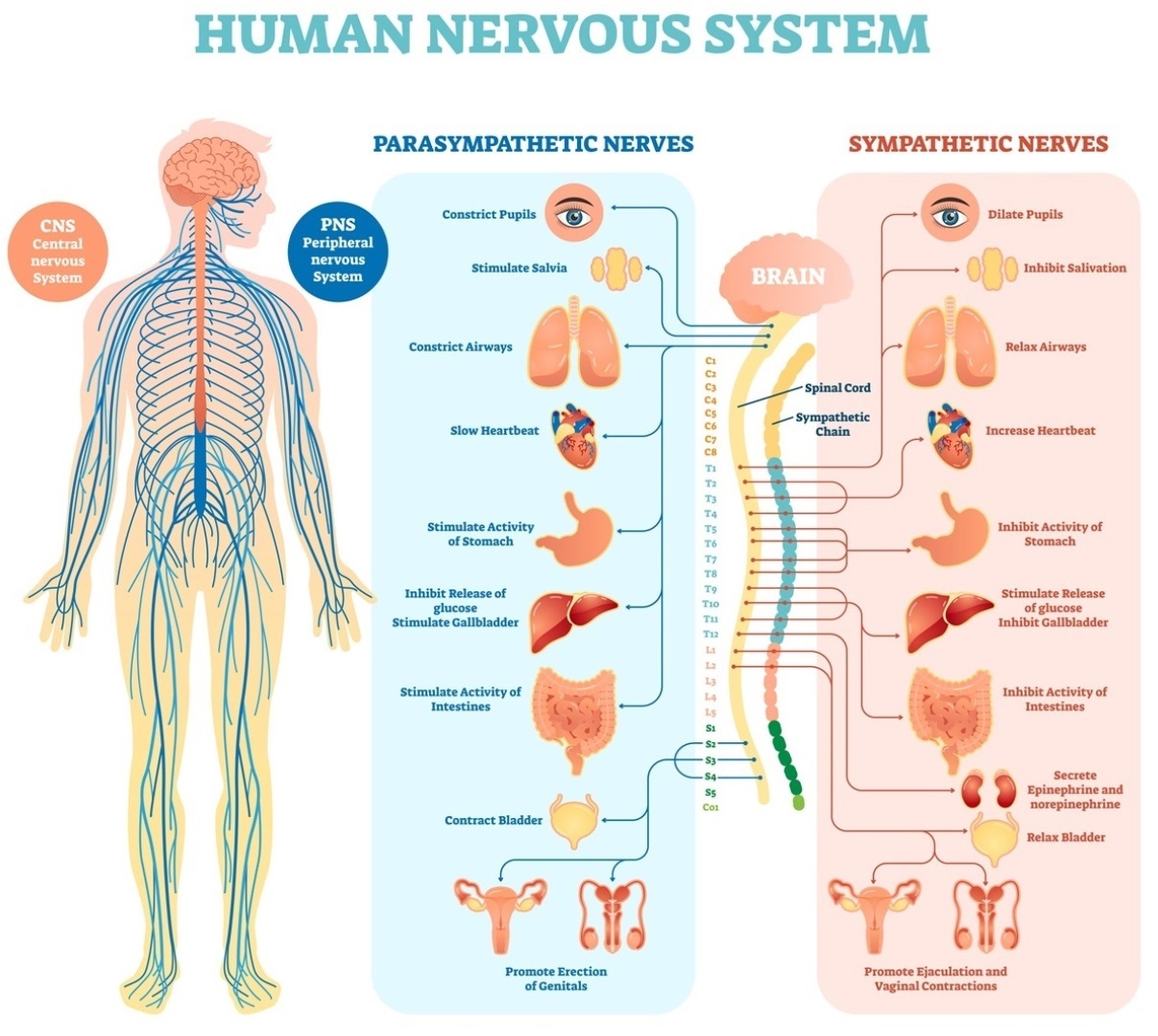
Sympatikus:
neurotransmiter:
- adrenalin, noradrenalin
srdce a cévy:
- zesílení kontraktility srdce
- zrychlení srdeční akce
- zůžení cév periferie
- rozšíření cév kosterního svalstva
plíce
- relaxace svalů trachey a bronchů
- inhibice sekrece žláz z bronchů
GIT
- relaxace svalů střev
- snížení motility střev
- svěrače: kontrakce/relaxace
- slabá stimulace sekrece slinných žláz
Urogenitální trakt
- relaxace m. detrusor
- kontrakce sfinkterů
Oko
- zvýšení nitroočního tlaku
- mydriasa (rozšíření zornic)
- akomodace na dálku
- slabá stimulace sekrece slzných žláz
Játra
- glykogenolýza
- glukoneogeneze
Parasympatikus:
neurotransmiter:
- acetylcholin
srdce a cévy:
- zeslabení kontraktility srdce
- zpomalení srdeční akce
- rozšíření cév periferie (zanedbatelná)
- zůžení cév kosterního svalstva
plíce
- kontrakce svalů trachey a bronchů
- stimulace sekrece žláz z bronchů
GIT
- zvýšení tonu svalů střev
- zvýšení motility střev
- svěrače: relaxace
- silná stimulace sekrece slinných žláz
Urogenitální trakt
- kontrakce m. detrusor
- relaxace sfinkterů
Oko
- snížení nitroočního tlaku
- miosa (zůžení zornic)
- akomodace na blízko
- silná stimulace sekrece slzných žláz
FREEZE
Specifický druh reakce freeze - ztuhnutí - parasympatická reakce (zadní parasympatická větev n. vagus), spouští se ve chvíli, kdy organizmus vyhodnotí, že ohrožení je tak enormní, že ho nebude možné nijakými prostředky zvládnout, s ohrožením nelze bojovat, ani mu utéct. tzv. “Mrtvý brouk”
- vývojově starší strategie
- chrání organizmus před přívalem silných emocí, které by neměl pod kontrolou, před bolestí
- ztuhlost, strnulost, omezení pohybu, zblednutí, ledové končetiny, zpomalení fyziologických funkcí, chvění, hypomimie, emoce nejsou projevovány, ani pociťovány, snížené vnímání těla, derealizace, depersonalizace, disociace (odpojení) od emočního a tělesného prožívání.
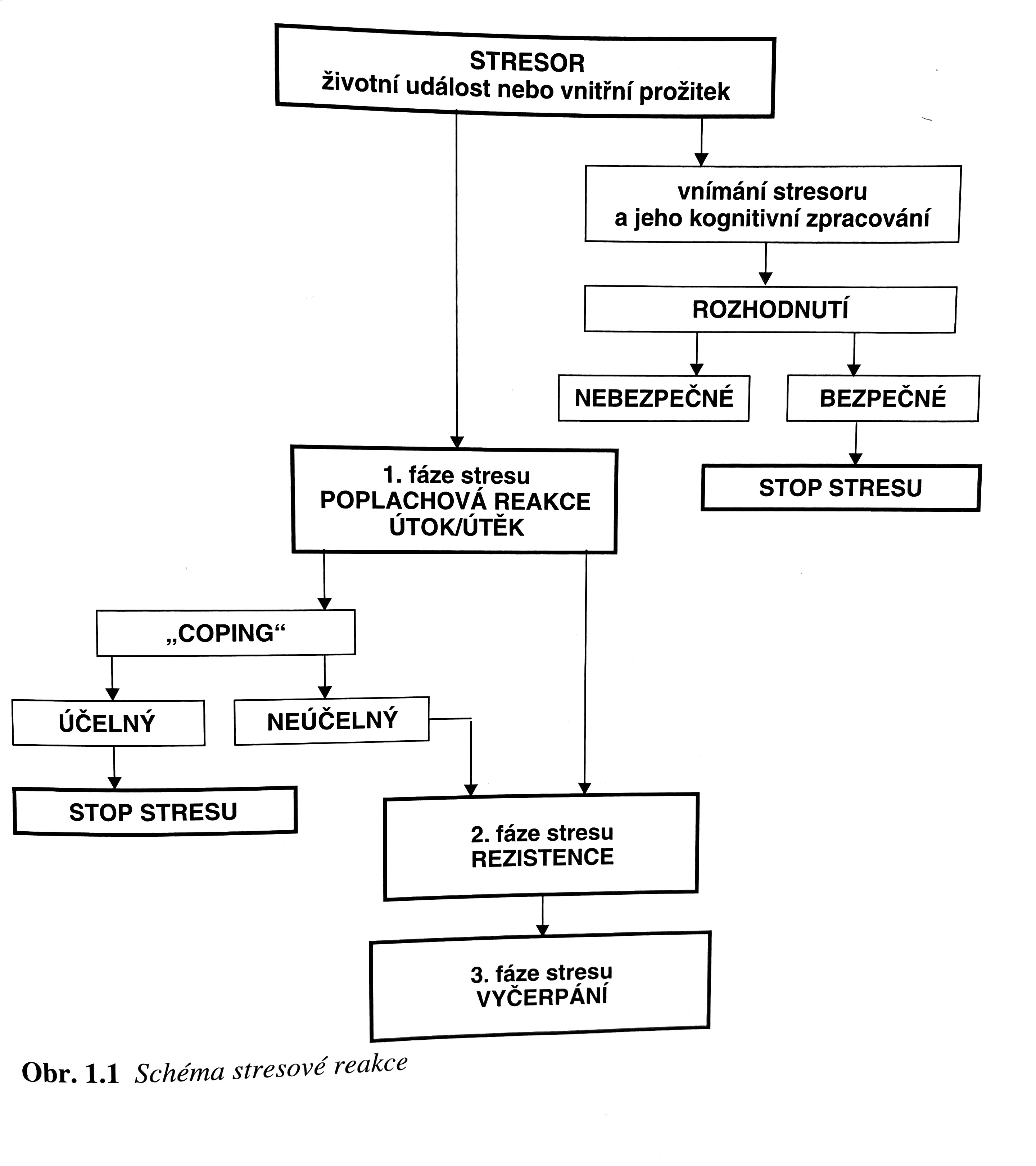
Po odeznění stresoru zpětnovazebným systémem vysoká hladina kortizolu působící na hypotalamus inhibuje další sekreci kortizolu. Snížená odpověď na tento stimul, nebo neodeznívání stresoru a dlouhá doba trvání stresu stimulují okruh, který vede k rezistenci na kortizol. Tím dochází k HPA hyperaktivitě. Chronický stres vede globálně k snížené expresi BDNF a k snížené schopnosti neurogeneze. Dále vede k poškození funkce hipokampu a k hipokampální atrofii, co dál prohlubuje dysregulaci HPA osy.
Pokud stres přetrvává a dochází dál k hyperstimulaci limbického systému dochází časem k fázi vyčerpání, nebo rezignace. V této fázi se vypíná standardní sympatická odpověď a převládá aktivace parasympatiku která vede ke zpomalení, strnutí, ztuhnutí, někdy k disociaci, odpojení od emocí.
Tento mechanizmus přispívá k patogenezi úzkostných poruch, deprese, somatizace, z dlouhodobého hlediska může přispívat k rozvoji demence.
Stres je negativním neurovývojovým faktorem. V dětství je mozek citlivý na působení neurotoxických kortikoidů. Kojenci ještě nemají vyvinutý parasympatikus a neumí se sami zklidnit. Na ztišení je nutná přítomnost láskyplné pečující osoby. Pečující osoba tonizuje nervový systém dítěte a má velký vliv na jeho emoční reaktivitu v dospělosti.
Když o děti není dobře pečováno, ovlivňuje to přední cingulum (oblast odpovědnou za empatii a péči o druhé), je bohatá na opioidní receptory, aktivuje se při zažívání bolesti, jak psychické tak i fyzické. Absence péče vede k chronické bolesti až disociaci.
Integrace prožitků a disociace
Za normálních okolností a za situace normálního nabuzení fungují hot systém a cool systém v rovnováze, co vede k integraci prožívané skutečnosti. Většinou si uvědomujeme co se děje, co si o tom myslíme, jaké kolem toho máme emoce, co vnímáme na senzorické a tělesné úrovni, jak dlouho to trvá, a že se to děje nám, co k tomu vedlo a plánujeme jak se k tomu postavíme do budoucna.
- “HOT” systém: Systém amygdaly je odpovědný za IMPLICITNÍ složku prožování - emoční, tělesné, neverbální vjemy, které nás hluboce ovlivňují ale nemusíme si je uvědomovat, zprostředkovává propojení s ranými tělesnými a emočními vzpomínkami, které jsou fragmentované, bez racionální kauzality a nemají časový sled. Tento implicitní systém emočního reagování je vývojově starší a rychlejší.
- “COOL “systém: Systém hipokampu a kortexu je odpovědný za EXPLICITNÍ složku prožívání - racionální vyhodnocování a pojmenovávání situace, dávání do souvislostí, časových sledů. Je odpovědný za uvědomování si myšlenek, emocí, senzorických prožitků a za integraci toho, co se děje, kdy se to děje, komu se to děje. Důležitou roli má thalamus (propojen s limbickým systémem a s mozkovou kůrou), který je odpovědný za zpracovávání smyslových vjemů a je odpovědný za vytvoření koherentní zkušenosti “toto se mi teď děje a jsem si toho vědom”. Tento systém je vývojově mladší a pomalejší, než implicitní systém.
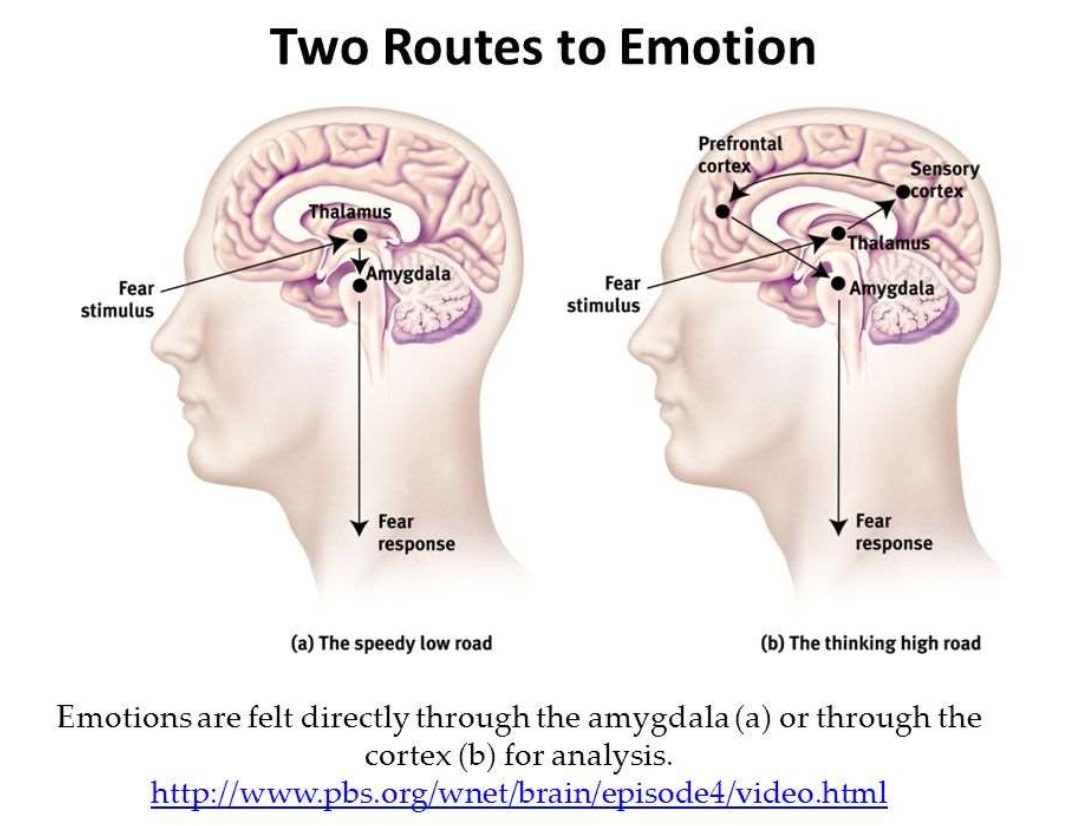
V situacích intenzivního emočního prožívání, kdy dochází k zaplavení emocemi je dominantní implicitní systém a explicitní systém je umlčován (je náročné přemýšlet, racionálně rozvážně reagovat). Naopak při dominanci explicitního racionálního systému, si můžeme zcela přestat uvědomovat svoje emoční prožívání. Jeden systém při přílišné aktivaci vytlačuje druhý.
Za situací extrémního emočního vypětí u traumatizujících zážitků může dojít k úplnému rozpojení těchto dvou systémů - DISOCIACI- a je narušená integrace prožívání, myšlení, cítění, identity. Na událost je amnézie (není epizodická paméťová stopa) ale zároveň je prožitek uložen na implicitní emoční a tělesné úrovni a dál negativně ovlivňuje jedince.
TRAUMA
Zážitek, který téměř u každého vyvolá pronikavou tíseň a výraznou stresovou reakci.
Jde o události ohrožení života, zdraví, tělesné či psychické integrity nebo nejdůležitějších hodnot. Událost se stává traumatickou, když překročí schopnost člověka ji emočně zvládnout.
Jedinec zakouší extrémní strach, bezmoc, nebo hrůzu v určitém časovém úseku události.
Rozdělení traumatických zážitků:
- Monotrauma (nehody, úrazy, přírodní katastrofy, bolestivé lékařské zákroky, traumatické ztráty, přepadení, okradení, znásilnění, teroristický útok)
- Komplexní trauma (domácí násilí, týrání, sexuální zneužívání, válka, zajetí, mučení, migrace, extrémní chudoba)
- Vývojové trauma (ztráta pečující osoby, zanedbávání, fyzické či psychické týrání, sexuální zneužívání, závislosti rodičů, ztráta zdraví, silná bolest, rozvod, dlouhodobá devalvace, šikana ve škole, pre/peri/postnatální stres, někto blízký ve vězení)
- K vývojovému traumatu můžou vést tzv. ACE. Adverse child experiences nepříznivé dětské zkušenosti - takové zážitky, které dítěti způsobí dlouhodobě vysokou míru stresu, následky se nemusí projevit hned často se projeví až v dospělosti.
- Zvyšují v budoucnu riziko promiskuity, zneužívání alkoholu a drog, špatného prospěchu, úzkostí, depresí, pokusů o sebevraždu, autoimunitních onemocnění, infarktů, mrtvic, diabetu, rakoviny.
Neurobiologické změny po traumatu
- Dysregulace HPA osy, převaha tonu sympatiku
- Hormonální změny
- Funkční a morfologické změny mozku a jednotlivých struktur (aktivita, konektivita, velikost)
- Zvýšená aktivace amygdaly, nepropojuje se dobře s kortexem
- Zmenšení objemu hipokampu
- Insula = místo vnímání svého těla, narušené, člověk pak vlastně nevnímá, jak se tělo cítí, „necítí se dobře“
- menší objem mozečku, corpus callosum, šedé hmoty v určitých oblastech kůry, oslabený prefrontální kortex, formují se i abnormní synaptické spoje
- změny v thalamu = syntéza vjemů, integrace senzorických jader, filtr pro pozornost, u PTSD nefunguje, konstantní senzorické přetížení (nebo pak totální záklopka
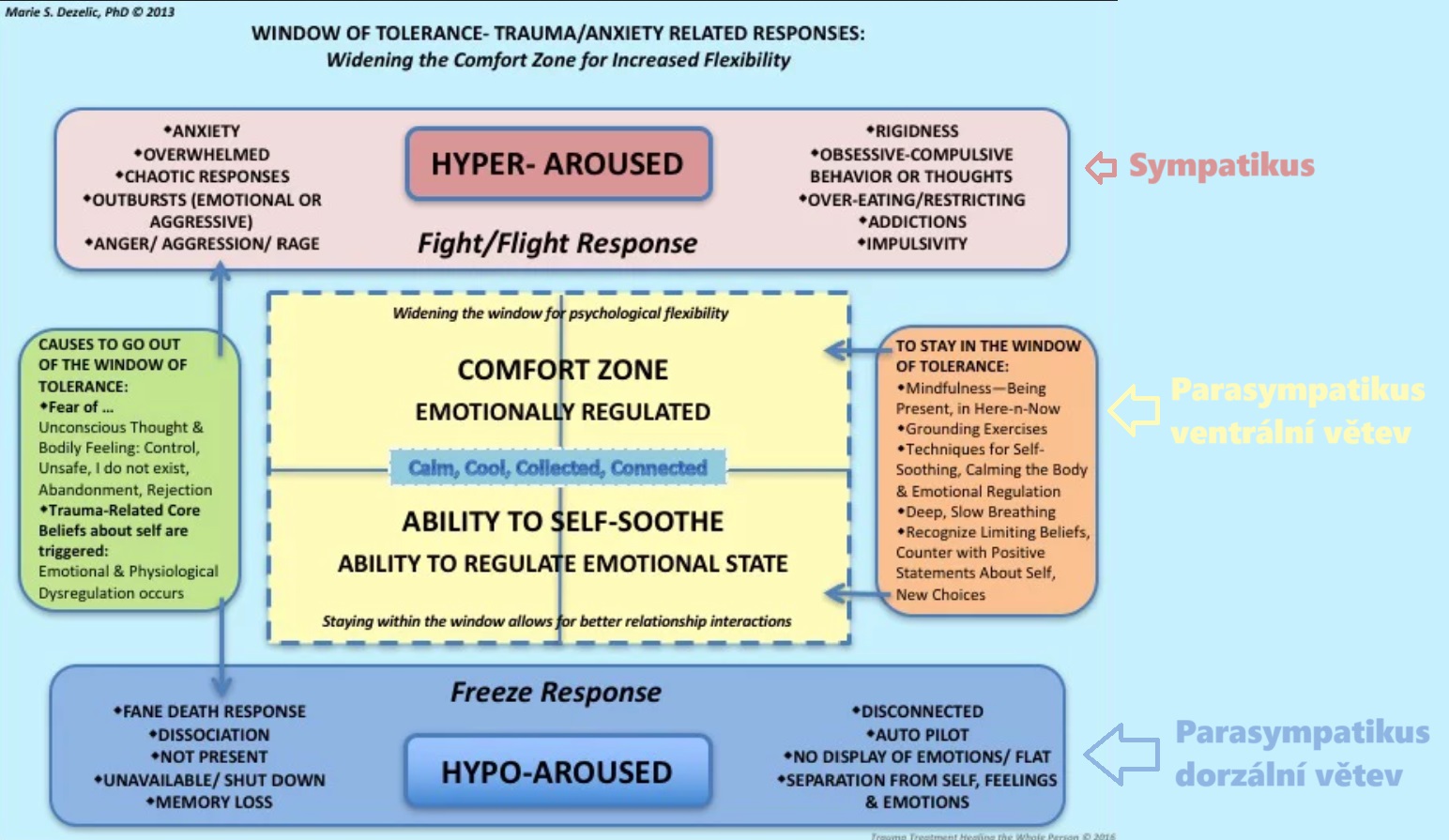
Zóna optimálního nabuzení mozku “comfort zone” je taková míra nabuzení, při které se cítíme bezpečně, jsme zvědaví, dobře naladění, připravení družit se s ostatními a explorovat svoje okolí. Traumatizace vede k vychýlení funkčního propojení mozku takovým způsobem, že je častěji vychýlená z této komfortní zóny, nebo je tato komfortní zóna extrémně zůžená.